
����Ŀ��ij��ȤС��ͬѧ��ʵ�����ü���1-������ŨH2SO4���廯�ƻ����ķ������Ʊ�1-�嶡�飬�����鷴Ӧ�IJ��ָ�����������ͼ��ʾװ�ã����мг�������������������ȴˮ��û�л�����
��֪��NaBr+H2SO4=NaHSO4+HBr
��CH3(CH2)2CH2OH+HBr![]() CH3(CH2)2CH2Br+H2O
CH3(CH2)2CH2Br+H2O
����Ӧ�������
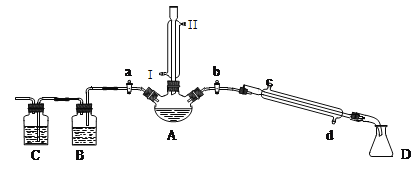
�����ʵ�鲽�裬�ش��������⣺
��1���ر�a��b����ͨ��ֱ�����ܵ�����ˮ����A����30���ӣ��Ʊ�1-�嶡�顣��ֱ�����ܽ�ͨ����ˮ����ˮ����_____(�I����)��������������ҪĿ����________��
��2�������ϣ�������Ӧ�ĸ���������У�����(CH3CH2CH2CH2-O-CH2CH2CH2CH3)��1-��ϩ���廯�⡢�������ơ�ˮ�ȡ�Ϩ��ƾ��ƣ�����ֱ�������Ϸ��������Ӳ���a���������ȼ�����Ӧֱ����ȴ��ͨ��B��Cװ�ü��鲿�ָ�����B��C��Ӧʢ�ŵ��Լ��ֱ���ʯ�����ˮ��Bװ�ó���ʯ�ﻹ����______(���Լ�����)д��Cװ������Ҫ�Ļ�ѧ����ʽ��_________________________________________________��
��ͬѧ��ͨ����������Ǽ������ò������Ƿ�������CH2CH2CH2CH3���� ��ȷ���������д��ڶ��ѡ�����Ը�ͬѧ�Ĺ۵��������________________________________��
��3��Ϊ�˽�һ�������ᴿ1-�嶡�飬����ȤС��ͬѧ�������л�������������ʾ��
���� | �۵�/�� | �е�/�� |
1-���� | -89.5 | 117.3 |
1-�嶡�� | -112.4 | 101.6 |
���� | -95.3 | 142.4 |
1-��ϩ | -185.3 | -6.5 |
���㲹������ʵ�鲽�裬ֱ�������1-�嶡�顣
�ٴ���ƿ��ȴ��ȥ��ֱ�������ܣ�
�ڲ��ϴ���Ƥ�����¶ȼƣ�
�۹ر�_______����_______��
�ܽ�ͨ�����ܵ�����ˮ��ʹ��ˮ��______�����룻
��Ѹ�������¶���_______�棬�ռ�������֡�
��4����ʵ������ȡ1-������NaBr�ֱ�Ϊ7.4 g��13.0 g�������Ĵֲ��ᆳϴ�ӡ�������ٴ�����õ�10.96 g 1-�嶡�飬��1-�嶡��IJ�����_____��������2λ��Ч���֣�
���𰸡� �� ��߷�Ӧ���ת���� ��������Һ CH3CH2CH=CH2+Br2��BrCH2CHBrCH2CH3 �÷�����������Ϊ1-�嶡����Ҳ����CH2CH2CH2CH3 a b d�� 101.6 80%
����������1���ر�a��b����ͨ��ֱ�����ܵ�����ˮ��Ӧ��Ҫ����������ȴ�����ˮ��ΪI����A����30���ӣ��Ʊ�1-�嶡�飮������������ҪĿ���dz�����÷�Ӧ���߷�Ӧ���ת��������2�������ϣ�������Ӧ�ĸ���������У����ѡ�1-��ϩ���廯�⡢�������ơ�ˮ�ȣ���ͨ��װ��B��C������������壬Ӧ����1-��ϩ���廯��Ĵ��ڣ��ȼ����廯��Ĵ�����ʯ����Һ����������Һ���飬ͨ��ʯ����Һ��Һ���ɫ����ͨ����������Һ����dz��ɫ������֤���廯������ɣ������1-��ϩ��ѡ���Լ�Ϊ��ˮ����������Һ��ͨ����ˮ����������Һ��ɫ֤�����ɵIJ����к���1-��ϩ��Cװ������Ҫ�Ļ�ѧ����ʽΪCH3CH2CH=CH2+Br2��BrCH2CHBrCH2CH3������1-�嶡����Ҳ����CH2CH2CH2CH3�����Ը÷�������������3���ᴿ1-�嶡�飬�ռ��������Ϊ1-�嶡�飬�����뽫1-�嶡������������Һ�����������¶ȴ���е�101.6�棬��������ԭ����װ����ƵIJ���Ϊ���ٴ���ƿ��ȴ��ȥ��ֱ�����������ڲ��ϴ���Ƥ�����¶ȼ����۹ر�a����b���ܽ�ͨ�����ܵ�����ˮ��ʹ��ˮ��d����������Ѹ�������¶���101.6�����ռ������������4�����ݻ�ѧ����ʽ��֪
CH3CH2CH2CH2OH+NaBr+H2SO4![]() CH3CH2CH2CH2Br+NaHSO4+H2O
CH3CH2CH2CH2Br+NaHSO4+H2O
74 103
7.4g 10.3g
�廯�ƹ�������1-����ȫ����Ӧ����1-�嶡�����ʵ���Ϊ0.1mol������Ϊ0.1mol��137g/mol=13.7g�������Ĵֲ��ᆳϴ�ӡ�������ٴ�����õ�10.96g 1-�嶡�飬���Բ���Ϊ10.96g/13.7g��100%=80%��


 ��˼ά������ҵ���ټ��ִ�ѧ������ϵ�д�
��˼ά������ҵ���ټ��ִ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼװ����ʾ��C��D��E��F��X��Y��Ϊ���Ե缫���ס�������Һ�����Ϊ500mL����ҺŨ�Ⱦ���ͬ(����ͨ��ǰ����Һ�������)��A��BΪ���ֱ����Դ����������ֱ����Դ��ͨ��F�������ʺ�ɫ����ش�

��1��B���ǵ�Դ��_____����һ��ʱ�������Һ��ɫ��____������X����������ɫ��dz��Y����������ɫ��������Fe(OH)3��������____�ɡ�
��2�����һ��ʱ���ס���װ���е�C��D��E��F�缫���ֱ�ֻ��һ�ֵ�������ʱ����Ӧ���ʵ����ʵ���֮��Ϊ______________�����з�����Ӧ�Ļ�ѧ����ʽΪ__________________________________����Ҫʹ����ļ�װ���е���Һ�ָ���ԭŨ���������һ������_________(�ѧʽ)��
��3�����ñ�װ�ø�ͭ����������HӦ����______(�����Ʋ�����������Ƽ���)�����Ƽ�������5.4g��ʱ�� �ס�������Һ��pH�ֱ�Ϊ_____��_____
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ֶ�����Ԫ��X��Y��Z��Wԭ������������������Y�ǹ���������������һ��Ԫ�ء�m��n��p��Ϊ����ЩԪ����ɵĶ�Ԫ������ס��ҡ�������������Ԫ�ض�Ӧ�ĵ��ʣ�m�������ǡ�����������Ļ����У�ǿ�������������ҡ���n��ʹʪ��ĺ�ɫʯ����ֽ�������������ʵ�ת����ϵ��ͼ��ʾ(��Ӧ��������ȥ)������˵����ȷ����

A. ���³�ѹ�£�X��Y��ɵĻ�����һ��Ϊ����
B. X��Z��W����Ԫ�ز���������ӻ�����
C. ԭ�Ӱ뾶��X<W<Y<Z
D. ͼʾת����ϵ���漰�ķ�Ӧ��Ϊ������ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ���ֻ�����Ľṹ������������ȷ����( )
��A��B�ķ���ʽ��ΪC10H14O2���ǻ�Ϊͬ���칹�壻 ���������ʽΪC9H12O2���л���һ��Ϊͬϵ��
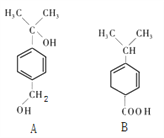
��A��B�����й�ƽ���̼ԭ������ͬ
��A��B����ʹ���Ը��������Һ��ɫ
�����ú�������������������ú˴Ź�����������A��B
��A��B���������ֹ�����
��1molA���������������Ʒ�Ӧ��1molB�������ı���̼��������Һ��Ӧ������������ʵ���Ϊ2:1
��1molB��1molBr2�����ӳɷ�Ӧ���������ֲ�ͬ����������ֲ��ﻥΪͬ���칹��
A. �٢ڢۢܢݢޢ� B. ֻ�Тۢޢ� C. ֻ�Т� D. ֻ�Тۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������벻�����ѧ���ʣ���������������������ǣ� ��
A.�ռ�
B.ˮ��
C.����
D.���ʯ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���Fe�� OH��3�����˵���У�����ȷ���ǣ� ��
A.��ɢ������ֱ����10��9��l0��7m֮��
B.��һ�ִ�����
C.���ж����ЧӦ
D.���о�ˮ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��![]() ��һ���л��ϳɵ��м��壬����ͨ������;�����ϳɣ�
��һ���л��ϳɵ��м��壬����ͨ������;�����ϳɣ�

��֪��(1) 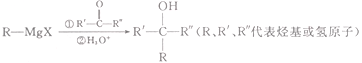
(2) 
(3) ![]()
�ش��������⣺
(1)M�ķ���ʽΪ__________________��
(2)N��ϵͳ������������Ϊ_____________________��
(3)D�й���������Ϊ__________________��
(4)��A����B�Ļ�ѧ����ʽΪ___________________����Ӧ����Ϊ________________��
(5)H�DZ�G��6��̼ԭ�ӵ�G��ͬϵ���H��_________�֣����к˴Ź����������������շ�Ľṹ��ʽΪ___________________��
(6)д�����ȱ�Ϊԭ���Ʊ������� �ĺϳ�·�ߣ�______________________��(�����Լ���ѡ)��
�ĺϳ�·�ߣ�______________________��(�����Լ���ѡ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д��ȷ����
A. �����ܽ�ˮ����CH3COOH+CaCO3��CH3COO��+H2O+CO2
B. ��NH4Fe(SO4)2��Һ�м�������Ba(OH)2��Һ��2Fe3+ + 3SO42��+ 3Ba2+ + 6OH��=== 3BaSO4��+ 2Fe(OH)3��
C. ������þ�����ᷴӦ��H����OH��===H2O
D. Ba(OH)2��Һ�м������NH4HSO4��Һ�� Ba2����2OH����NH4����H����SO42��=== BaSO4��NH3��H2O��H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����50 mL NaOH��Һ����ͨ��һ������CO2(������Һ�������)�����ȡ����Һ10 mL������ϡ����100 mL�������ϡ�ͺ����Һ����μ���0.1 mol��L-1���ᣬ����CO2��������(��״����)������������������ϵ����ͼ��ʾ��

(1) д��OA����������Ӧ�����ӷ���ʽ��______________��
(2)NaOH������CO2��������Һ������Ϊ____�������ʵ���Ũ��֮��Ϊ____��
(3)����CO2�����(��״����)Ϊ____��
(4)ԭNaOH��Һ�����ʵ���Ũ��Ϊ___��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com