
【题目】综合利用海水可以制备食盐、纯碱、金属镁、溴等物质,其流程如下图所示:
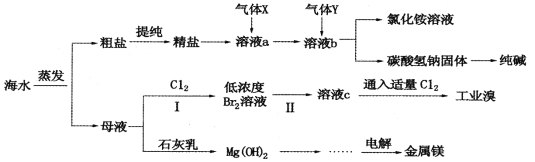
(1)利用海水可制备C12,为便于储存,可将C12液化,应采取的措施之一是__________。
(2)粗盐中含有硫酸钠、氯化镁、氯化钙等可溶性杂质,为除去这些杂质而得精盐,进行如下操作:①溶解 ②加过量的BaCl2溶液 ③加过量的NaOH溶液 ④加过量的Na2CO3溶液 ⑤_________(填操作名称,下同) ⑥加适量的盐酸 ⑦___________。
(3)气体X为___________。溶液b中发生反应的化学方程式是______________________。
(4)步骤I中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为_________________。步骤Ⅱ中通入空气吹出Br2,用SO2水溶液进行吸收,得到溶液c,反应的离子方程式为__________________。在实验室中,从工业溴中提取溴单质的实验操作名称是____________。
(5)工业上制取金属镁的化学方程式为________________________。
【答案】(1)降温(或加压);(2)过滤;蒸发结晶
(3)NH3;;NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl
(4)富集溴元素;SO2+Br2+2H2O=4H++SO42-+2Br-;萃取;
(5)MgCl2=通电=Mg+Cl2↑
【解析】
试题分析:(1)氯气的沸点比较低,液化时需降温或加压处理。
(2)为了防止产生的沉淀,重现溶解,因此在加盐酸之前,应先过滤;从溶液中得到氯化钠固体,采用蒸发结晶的方法;
(3)上述流程是制取纯碱,制取纯碱的反应方程式为NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl,因为氨气极易溶于水,且溶于水后溶液显碱性,这样能更好充分利用二氧化碳,因此先通入氨气。
(4)步骤I中获取的溴浓度较小,步骤 II又将Br2还原为Br-,其目的为富集溴元素;其离子方程式为SO2+Br2+2H2O=4H++SO42-+2Br-;在实验室中,从工业溴中提取溴单质的实验操作名称是萃取。
(5)工业上用电解氯化镁的方法制取镁,化学方程式为MgCl2=通电=Mg+Cl2↑


科目:高中化学 来源: 题型:
【题目】加热N2O5依次发生的分解反应为:①N2O5(g)![]() N2O3(g)+O2(g); ②N2O3(g)
N2O3(g)+O2(g); ②N2O3(g)![]() N2O(g)+O2(g)在容积为2L的密闭容器中充入8mol N2O5,加热到t℃,达到平衡状态后O2为9mol,N2O3为3.4mol,则t℃时反应①的平衡常数为( )
N2O(g)+O2(g)在容积为2L的密闭容器中充入8mol N2O5,加热到t℃,达到平衡状态后O2为9mol,N2O3为3.4mol,则t℃时反应①的平衡常数为( )
A. 10.7 B.8.5 C.9.6 D.10.2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B两种烃,它们含碳质量分数相同,下列关于A和 B的叙述正确的是
A.A和 B一定是同分异构体 B.A和 B不可能是同系物
C.A和 B最简式一定相同 D.A和 B的化学性质相似
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于乙烯的说法中错误的是
A.乙烯可以催熟植物的果实
B.乙烯生成聚乙烯的反应是乙烯分子互相加成反应
C.聚乙烯由乙烯聚合而成,故分子中含有很多碳碳双键
D.聚乙烯的单体是乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在室温下,向Cu(IO3)2饱和溶液中加入足量的经稀硫酸酸化的KI溶液,产生碘化亚铜(CuI)沉淀,溶液由蓝色变为棕黄色,反应前加入淀粉溶液不变蓝,反应后加入淀粉溶液变为蓝色。
(1)该反应中氧化剂是__________;
(2)该反应的氧化产物是__________;
(3)1mol氧化剂在反应中得到电子的物质的量为__________;
(4)某反应体系中有物质:Bi2(SO4)3、NaMnO4、H2O、MnSO4、NaBiO3、Na2SO4、H2SO4 。请将NaBiO3之外的反应物与生成物分别填入以下空格内,配平化学计量数,并用单线桥表示电子转移的方向和数目。
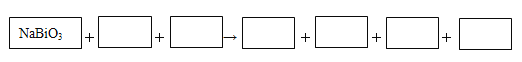
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列说法正确的是( )
A. 22.4 L O2的质量约为32g
B. 17g NH3所含原子数为4NA,所含电子数为10NA
C. 标准状况下,22.4LH2O所含水分子为NA个
D. 0.5 mol/L Fe2(SO4)3 溶液中,SO42-的数目为1.5 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“神舟七号”的燃料是氢化锂三兄弟——LiH、LiD、LiT。其中Li的质量数为7,对这三种物质的下列说法正确的是
A. 质子数之比为1:2:3 B. 中子数之比为1:1:1
C. 摩尔质量之比为8:9:10 D. 化学性质不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活息息相关,下列叙述错误的是( )
A.为防止电池中的重金属污染土壤和水体,应积极开发废旧电池的综合回收利用
B.氢能是清洁能源,工业上电解水法制大量氢气符合节能减排理念
C.大量的汽车尾气是造成雾霾天气的一个重要因素
D.煤的液化和气化均属于化学变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com