
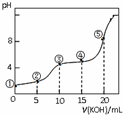
 常温下,用0.05mol•L-1 KOH溶液滴定 10.00mL0.05mol•L-1 H2C2O4(二元弱酸)溶液所得滴定曲线如图(体积变化忽略不计).下列说法错误的是( )
常温下,用0.05mol•L-1 KOH溶液滴定 10.00mL0.05mol•L-1 H2C2O4(二元弱酸)溶液所得滴定曲线如图(体积变化忽略不计).下列说法错误的是( )| A. | 点②溶液中:c(K+)+c(H+)=c(HC2O4-)+c(C2O42-)+c(OH-) | |
| B. | 点③溶液中:c(K+)=c(HC2O4-)+c(C2O42-)+c(H2C2O4) | |
| C. | 点④溶液中:c(K+)+c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.05 mol•L-1 | |
| D. | 点⑤溶液中:c(K+)>c(HC2O4-)>c(C2O42-)>c(OH-)>c(H+) |
分析 A.任何电解质溶液中都存在电荷守恒,根据电荷守恒判断;
B.该点溶液中溶质为任何电解质溶液中都存在物料守恒,根据物料守恒判断;
C.点④溶液中存在等物质的量浓度的K2C2O4和KHC2O4,根据物料守恒判断;
D.该点溶液中二者恰好完全反应,溶液中溶质为K2C2O4,草酸根离子水解导致溶液呈碱性,但其水解程度较小.
解答 解:A.任何电解质溶液中都存在电荷守恒,根据电荷守恒得c(K+)+c(H+)=c(HC2O4-)+2c(C2O42-)+c(OH-),故A错误;
B.二者恰好完全反应生成KHC2O4,该点溶液中溶质为任何电解质溶液中都存在物料守恒,根据物料守恒得c(K+)=c(HC2O4-)+c(C2O42-)+c(H2C2O4),故B正确;
C.点④溶液中存在等物质的量浓度的K2C2O4和KHC2O4,由物料守恒可知,c(K+)+c(H2C2O4)+c(HC2O4-)+c(C2O42-)=$\frac{0.05mol/L×(0.015+0.01)L}{(0.015+0.01)L}$=0.05mol•L-1,故C正确;
D.该点溶液中二者恰好完全反应,溶液中溶质为K2C2O4,草酸根离子水解导致溶液呈碱性,但其水解程度较小,所以c(HC2O4-)<c(C2O42-),故D错误;
故选AD.
点评 本题以酸碱混合定性判断为载体考查离子浓度大小比较,明确混合溶液中溶质及其性质、溶液酸碱性是解本题关键,会灵活运用电荷守恒和物料守恒,易错选项是C.


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:解答题
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | 0 |
| 2 | C | N | O | |||||
| 3 | Na | Mg | Si | S | Cl | Ar | ||
| 4 | Ca |
 ;Ca的最外层电子数为2.
;Ca的最外层电子数为2.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验及现象 | 结论 |
| A | 将湿润的红色石蕊试纸放在试管口,试纸变蓝 | 反应中有NH3产生 |
| B | 收集产生的气体并点燃,火焰呈淡蓝色 | 反应中有H2产生 |
| C | 收集气体的同时测得溶液的pH为8.6 | 溶液中OH?氧化了Mg |
| D | 将光亮的镁条放入pH为8.6的NaHCO3溶液中,有气泡产生 | 弱碱性溶液中Mg也可被氧化 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Fe3++SO32-+H2O→2Fe2++SO42-+2H+ | |
| B. | I2+SO32-+H2O→SO42-+2I-+2H+ | |
| C. | 2Fe2++I2→2Fe3++2I- | |
| D. | Br2+SO32-+H2O→SO42-+2Br-+2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
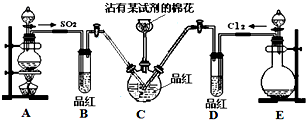 探究SO2和氯水的漂白性,设计了如下实验,装置如图.
探究SO2和氯水的漂白性,设计了如下实验,装置如图.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com