

 ,OPA分子中最多有16个原子共平面.
,OPA分子中最多有16个原子共平面.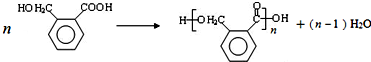 (不必注明反应条件),该反应的类型为缩聚反应.
(不必注明反应条件),该反应的类型为缩聚反应.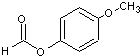 (写出其结构简式).
(写出其结构简式). 分析 A是摩尔质量为106g•mol-1的烃,A和溴发生取代反应生成C,根据C的结构简式知,A为邻二甲苯,其结构简式为 ,A和溴在铁作催化剂条件下发生取代反应生成B,根据B的分子式知,B的结构简式为
,A和溴在铁作催化剂条件下发生取代反应生成B,根据B的分子式知,B的结构简式为 ,C发生卤代烃的水解反应,再脱水后生成OPA为
,C发生卤代烃的水解反应,再脱水后生成OPA为 ,结合已知反应信息③可知,邻苯二甲醛反应生成D,D的结构简式为
,结合已知反应信息③可知,邻苯二甲醛反应生成D,D的结构简式为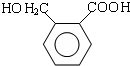 ,E是一种聚酯类高分子化合物,D发生缩聚反应生成E,则E的结构简式为
,E是一种聚酯类高分子化合物,D发生缩聚反应生成E,则E的结构简式为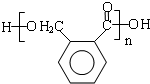 ,据此解答.
,据此解答.
解答 解:A是摩尔质量为106g•mol-1的烃,A和溴发生取代反应生成C,根据C的结构简式知,A为邻二甲苯,其结构简式为 ,A和溴在铁作催化剂条件下发生取代反应生成B,根据B的分子式知,B的结构简式为
,A和溴在铁作催化剂条件下发生取代反应生成B,根据B的分子式知,B的结构简式为 ,C发生卤代烃的水解反应,再脱水后生成OPA为
,C发生卤代烃的水解反应,再脱水后生成OPA为 ,结合已知反应信息③可知,邻苯二甲醛反应生成D,D的结构简式为
,结合已知反应信息③可知,邻苯二甲醛反应生成D,D的结构简式为 ,E是一种聚酯类高分子化合物,D发生缩聚反应生成E,则E的结构简式为
,E是一种聚酯类高分子化合物,D发生缩聚反应生成E,则E的结构简式为 ,
,
(1)根据上面的分析可知,A为邻二甲苯,
故答案为:邻二甲苯;
(2)B的结构简式为 ,检验B中溴元素的方法正确是滴加NaOH溶液共热,后加稀硝酸酸化,再加硝酸银溶液,观察有无浅黄色沉淀,
,检验B中溴元素的方法正确是滴加NaOH溶液共热,后加稀硝酸酸化,再加硝酸银溶液,观察有无浅黄色沉淀,
故选d;
(3)根据上面的分析可知,OPA为 ,由于苯环上所有原子共面,碳氧双键上所有原子也共面,所以OPA分子中最多有16个原子共平面,
,由于苯环上所有原子共面,碳氧双键上所有原子也共面,所以OPA分子中最多有16个原子共平面,
故答案为: ;16;
;16;
(4)D的结构简式为 ,D中官能团的名称是 羟基、羧基,由D生成E的化学反应方程式为
,D中官能团的名称是 羟基、羧基,由D生成E的化学反应方程式为 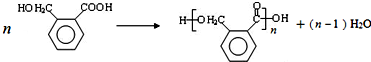 ,该反应的类型为缩聚反应,
,该反应的类型为缩聚反应,
故答案为:羟基、羧基;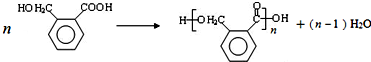 ;缩聚反应;
;缩聚反应;
(5)D为 ,D的同分异构体中含有苯环且苯环上的取代基至少有两个,能水解且能发生银镜反应,即有甲酸某酯,则符合条件的结构为苯环上连有两个取代基,为-CH2OH、-OOCH,或-OH、-CH2OOCH,或-OCH3、-OOCH,分别有邻间对三种,共有9种,也可以是三个取代基,为,有10种,所以共有19种,其中核磁共振氢谱为4组峰,且面积之比为l:2:2:3的是
,D的同分异构体中含有苯环且苯环上的取代基至少有两个,能水解且能发生银镜反应,即有甲酸某酯,则符合条件的结构为苯环上连有两个取代基,为-CH2OH、-OOCH,或-OH、-CH2OOCH,或-OCH3、-OOCH,分别有邻间对三种,共有9种,也可以是三个取代基,为,有10种,所以共有19种,其中核磁共振氢谱为4组峰,且面积之比为l:2:2:3的是  ,
,
故答案为:19; .
.
点评 本题考查有机物的推断,明确有机物的官能团及其性质是解本题关键,侧重考查学生分析推理能力与知识迁移应用,难度中等,(5)中同分异构体的书写为易错点、难点.


科目:高中化学 来源: 题型:选择题
| A. | 用酸性高锰酸钾溶液鉴别乙烷和乙烯 | |
| B. | 用分液漏斗分离乙醛和水 | |
| C. | 用苯、溴水和铁粉混合制取溴苯 | |
| D. | 用紫色石蕊溶液检验苯酚弱酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化铁可用作红色油漆和涂料 | B. | 硅胶可作干燥剂 | ||
| C. | 纯碱可作糕点的发酵粉 | D. | 过氧化钠作呼吸面具供氧剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
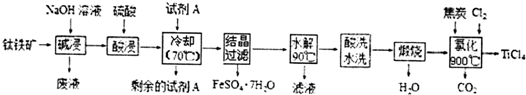
 铁在自然界分布广泛,在工业、农业和国防科技中有重要应用.回答下列问题:
铁在自然界分布广泛,在工业、农业和国防科技中有重要应用.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用(NH4)2Fe(SO4)2 溶液与过量NaOH反应制Fe(OH)2:Fe2++2OH-=Fe(OH)2↓ | |
| B. | 用稀氢碘酸溶液除去铁制品表面的铁锈:Fe2O3+6H+=2Fe3++3H2O | |
| C. | 向小苏打溶液中加入少量Ca(OH)2溶液反应:Ca2++2OH-+2HCO3-=CaCO3↓+2H2O+CO32- | |
| D. | 向NaClO溶液中滴入少量FeSO4溶液,反应的离子方程式为:2Fe2++ClO-+2H+═Cl-+2Fe3++H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蛋白质属于天然有机高分子化合物,没有蛋白质就没有生命 | |
| B. | HCHO溶液或(NH4)2SO4溶液均能使蛋白质变性 | |
| C. | 某些蛋白质跟浓硝酸作用会变黄 | |
| D. | 可以采用多次盐析或多次渗析的方法分离、提纯蛋白质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
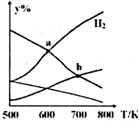 以CO2和H2为原料制取乙醇的反应为:2CO2(g)+6H2(g)═CH3CH2OH(g)+3H2O(g)△H<0.某压强下的密闭容器中,按CO2和H2的物质的量比为1:3投料,不同温度下,达到平衡后平衡体系中各物质的物质的量分数(y%)随温度变化如图所示.下列说法正确的是( )
以CO2和H2为原料制取乙醇的反应为:2CO2(g)+6H2(g)═CH3CH2OH(g)+3H2O(g)△H<0.某压强下的密闭容器中,按CO2和H2的物质的量比为1:3投料,不同温度下,达到平衡后平衡体系中各物质的物质的量分数(y%)随温度变化如图所示.下列说法正确的是( )| A. | a点的平衡常数小于b点 | B. | b点:v正(CO2)=v逆(H2O) | ||
| C. | a点:n(H2)=n(H2O) | D. | 温度不变,充入更多H2,D(CO2)不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com