
25 ℃时,将a mol/L的氨水与b mol/L盐酸等体积混合,下列有关推论不正确的是( )
A.若混合后溶液pH=7,则c(NH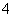 )=c(Cl-)
)=c(Cl-)
B.若b=2a,则c(Cl-)>c(NH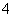 )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
C.若a=2b,则c(NH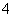 )>c(Cl-)>c(OH-)>c(H+)
)>c(Cl-)>c(OH-)>c(H+)
D.若混合后溶液满足c(H+)=c(OH-)+c(NH3·H2O),则可推出a=b
解析 溶液中存在c(Cl-)+c(OH-)=c(H+)+c(NH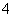
 ),因c(OH-)=c(H+),故c(NH
),因c(OH-)=c(H+),故c(NH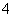 )=c(Cl-),A项正确;若b=2a,则混合溶液中的溶质为等物质的量的HCl和NH4Cl,由于NH
)=c(Cl-),A项正确;若b=2a,则混合溶液中的溶质为等物质的量的HCl和NH4Cl,由于NH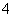 水解,故c(H+)>c(NH
水解,故c(H+)>c(NH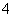 ),即c(Cl-)>c(H+)>c(NH
),即c(Cl-)>c(H+)>c(NH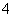 )>c(OH-),B项错误;若a=2b,则反应后生成的NH4Cl和剩余的NH3·H2O的物质的量相等,已知相同条件下NH3·H2O的电离程度大于NH
)>c(OH-),B项错误;若a=2b,则反应后生成的NH4Cl和剩余的NH3·H2O的物质的量相等,已知相同条件下NH3·H2O的电离程度大于NH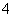 的水解程度,故混合溶液呈碱性,有c(NH
的水解程度,故混合溶液呈碱性,有c(NH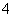 )>c(Cl-)>c(OH-)>c(H+),C项正确;若a=b,则完全反应生成NH4Cl,根据质子守恒可知c(H+)=c(OH-)+c(NH3·H2O),D项正确。
)>c(Cl-)>c(OH-)>c(H+),C项正确;若a=b,则完全反应生成NH4Cl,根据质子守恒可知c(H+)=c(OH-)+c(NH3·H2O),D项正确。
答案 B


 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案科目:高中化学 来源: 题型:
一定温度下的难溶电解质AmBn在水溶液中达到沉淀溶解平衡时,其Ksp=cm(An+)·cn(Bm-),称为难溶电解质的溶度积。25 ℃时,向AgCl的白色悬浊液中依次加入等浓度的KI溶液和Na2S溶液,观察到的现象是先出现黄色沉淀,最后生成黑色沉淀。已知所有的物质的颜色和溶度积如下表:
| 物质 | AgCl | AgI | Ag2S |
| 颜色 | 白 | 黄 | 黑 |
| Ksp(25 ℃) | 1.8×10-10 | 1.5×10-16 | 1.8×10-50 |
下列叙述中不正确的是( )
A.溶度积小的沉淀可以转化为溶度积更小的沉淀
B.若先加入Na2S溶液,再加入KI溶液,则无黄色沉淀产生
C.25 ℃时,饱和AgCl、AgI、Ag2S溶液中Ag+的浓度相同
D.25 ℃时,AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶度积相同
查看答案和解析>>
科目:高中化学 来源: 题型:
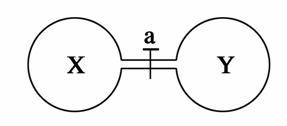
常温常压下,两个容积相同的烧瓶中分别盛满X和Y两种气体,打开开关a,使两烧瓶内的气体相通,最后容器内的压强由大到小的顺序排列正确的是( )
| 编号 | ① | ② | ③ | ④ |
| 气体X | HI | NH3 | H2 | NO |
| 气体Y | Cl2 | HCl | Cl2 | O2 |
A.②>③>①>④ B.③>①=④>②
C.③>①>④>② D.④>①>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
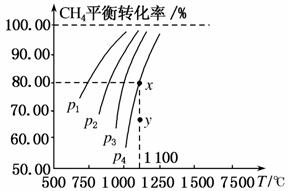
在一恒容的密闭容器中充入0.1 mol/L CO2、0.1 mol/L CH4,在一定条件下发生反应:CH4(g)+CO2(g)2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强关系如图,下列有关说法不正确的是( )
A.上述反应的ΔH<0
B.压强:p4>p3>p2>p1
C.1 100 ℃时该反应平衡常数为1.64
D.压强为p4时,在y点:v正>v逆
查看答案和解析>>
科目:高中化学 来源: 题型:
煤炭燃烧过程中会释放出大量的SO2,严重破坏生态环境。采用一定的脱硫技术可以把硫元素以CaSO4的形式固定,从而降低SO2的排放。但是煤炭燃烧过程中产生的CO又会与CaSO4发生化学反应,降低了脱硫效率。相关反应的热化学方程式如下:
CaSO4(s)+CO(g)CaO(s)+SO2(g)+CO2(g) ΔH1=+218.4 kJ·mol-1(反应Ⅰ)
CaSO4(s)+4CO(g)CaS(s)+4CO2(g)
ΔH2=-175.6 kJ·mol-1(反应Ⅱ)
请回答下列问题:
(1)反应Ⅰ能够自发进行的反应条件是________。
(2)对于气体参与的反应,表示平衡常数Kp时用气体组分(B)的平衡压强p(B)代替该气体物质的量的浓度c(B),则反应Ⅱ的Kp=________(用表达式表示)。
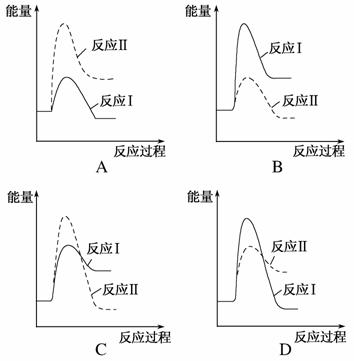
(3 )假设某温度下,反应Ⅰ的速率(v1)大于
)假设某温度下,反应Ⅰ的速率(v1)大于 反应Ⅱ的速率(v2),则下列反应过程能量变化示意图正确的是________。
反应Ⅱ的速率(v2),则下列反应过程能量变化示意图正确的是________。
(4)通过监测反应体系中气体浓度的变化可判断反应Ⅰ和Ⅱ是否同时发生,理由是____________________________________________________ ______________________________________________________________________________________
(5)图1为实验测得不同温度下反应体系中CO初始体积百分数与平衡时固体产物中CaS质量百分数的关系曲线。则降低该反应体系中SO2生成量的措施有________。
A.向该反应体系中投入石灰石
B.在合适的温度区间内控制较低的反应温度
C.提高CO的初始体积百分数
D.提高反应体系的温度
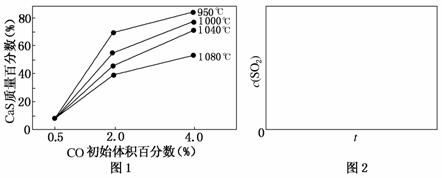
(6)恒温恒容条件下,假设反应Ⅰ和Ⅱ同时发生,且v1>v2,请在图2中画出反应体系中c(SO2)随时间t变化的总趋势图。
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是几种弱电解质的电离平衡常数、难溶电解质的溶度积Ksp(25 ℃)。
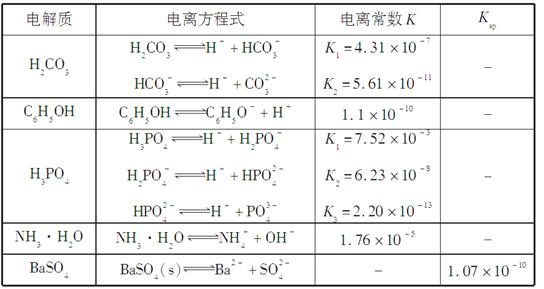
回答下列问题:
(1)写出C6H5OH与Na3PO4反应的离子方程式______________。
(2)25 ℃时,向10 mL 0.01 mol·L-1 C6H5OH溶液中滴加V mL 0.01 mol·L-1氨水,混合溶液中粒子浓度关系正确的是________(填选项字母)。
a.若混合液pH>7,则V≥10
b.V=5时,2c(NH3·H2O)+2c(NH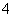 )=c(C6H5O-)+c(C6H5OH)
)=c(C6H5O-)+c(C6H5OH)
c.V=10时,混合液中水的电离程度小于0.01 mol·L-1 C6H5OH溶液中水的电离程度
d.若混合液pH<7,则c(NH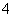 )>c(C6H5O-)>c(H+)>c(OH-)
)>c(C6H5O-)>c(H+)>c(OH-)
(3)水解反应的化学平衡常数称为水解常数(用Kh表示),类比化学平衡常数的定义。25℃时,Na2CO3第一步水解反应的水解常数Kh=________
mol·L-1。
(4)如图所示,有T1、T2不同温度下两条BaSO4在水中的沉淀溶解平衡曲线(已知BaSO4的Ksp随温度升高而增大)。
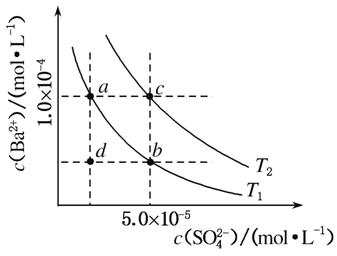
①T2________25 ℃(填“>”“<”或“=”)。
②讨论T1温度时BaSO4的沉淀溶解平衡曲线,下列说法正确的是________(填选项字母)。
a.加入Na2SO4不能使溶液由a点变为b点
b.在T1曲线上方区域(不含曲线)任意一点时,均有BaSO4沉淀生成
c.蒸发溶剂可能使溶液由d点变为曲线上a、b之间的某一点(不含a、b)
d.升温可使溶液由b点变为d点
查看答案和解析>>
科目:高中化学 来源: 题型:
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2 g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化曲线如图所示。下列分析错误的是( )
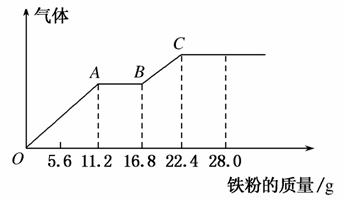
A.AB段的反应为:Fe+2Fe3+===3Fe2+
B.第二份溶液中最终溶质为FeSO4
C.混合酸中NO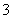 物质的量为0.4 mol
物质的量为0.4 mol
D.混合酸中H2SO4浓度为5 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知热化学方程式:
H2O(g)=H2(g) + 1/2O2(g) △H = +241.8kJ/mol
H2(g)+ 1/2O2(g) = H2O(1) △H = -285.8kJ/mol
当1g液态水变为水蒸气时,其热量变化是( )
A.吸热88kJ B. 吸热2.44KJ C.放热44kJ D. 吸热44KJ
查看答案和解析>>
科目:高中化学 来源: 题型:
当溶液中XO42- 和SO32- 的离子数之比为1∶2时,恰好完全发生氧化还原反应,X在还原产物中的化合价为 ( )
A、 +1 B、+2 C、+3 D、+4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com