
| A、Ag2O+H2O2═Ag+O2↑+H2O |
| B、H2O2═H2O+O2↑ |
| C、H2O2+Cr2(SO4)3+KOH═K2CrO4+K2SO4+H2O |
| D、Na2O2+HCl═H2O2+NaCl |


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
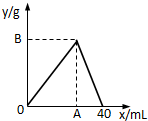 如图是表示往50mL AlCl3溶液中滴加4mol?L-1的NaOH溶液,生成沉淀的质量(y轴)与消耗NaOH溶液的体积(x轴)的关系.填空:
如图是表示往50mL AlCl3溶液中滴加4mol?L-1的NaOH溶液,生成沉淀的质量(y轴)与消耗NaOH溶液的体积(x轴)的关系.填空:查看答案和解析>>
科目:高中化学 来源: 题型:
| 实 验 混合溶液 | A | B | C | D | E | F |
| 4mol?L-1H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | 15 | 10 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B、由C(石墨)→C(金刚石)△H=+119 kJ?mol-1可知,石墨比金刚石稳定 |
| C、HCl和NaOH反应中和热△H=-57.3kJ/mol,则H2SO4和Ba(OH)2反应的中和热△H=2×(-57.3)kJ/mol |
| D、在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,则表示氢气燃烧热的热化学方程式为2H2(g)+O2(g)=2H2O(l)△H=-285.8 kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na→Na2O2 |
| B、Si→H2SiO3 |
| C、CuSO4→CuCl2 |
| D、Cu(OH)2→CuO |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X原子半径小于Y |
| B、X和Y的核电荷数之差为m-n |
| C、电负性X>Y |
| D、第一电离能 X<Y |
查看答案和解析>>
科目:高中化学 来源: 题型:
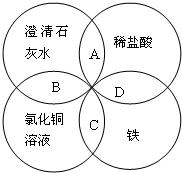 铁、稀盐酸、澄清石灰水、氯化铜溶液是中学化学中常见物质,四种物质间的反应关系如图所示.图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应反应的离子方程式书写正确的是( )
铁、稀盐酸、澄清石灰水、氯化铜溶液是中学化学中常见物质,四种物质间的反应关系如图所示.图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应反应的离子方程式书写正确的是( )| A、OH-+HCl=H2O+Cl- |
| B、Ca(OH)2+Cu2+=Ca2++Cu(OH)2↓ |
| C、Fe+Cu2+=Cu+Fe2+ |
| D、Fe+2H+=Fe3++H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、测定HCl和NaOH反应的中和热时,每次实验均应测量3个温度,即盐酸起始温度、NaOH起始温度和反应后终止温度 |
| B、在101 kPa时,1 mol H2完全燃烧生成液态水,放出285.8 kJ热量,H2的燃烧热为:-285.8kJ?mol-1 |
| C、在101 kPa时,1 mol C与适量O2反应生成1 mol CO时,放出110.5 kJ热量,则C的燃烧热为110.5 kJ?mol-1 |
| D、生成物总能量一定低于反应物总能量,同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com