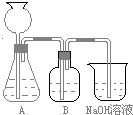
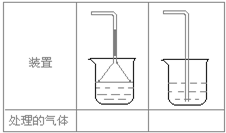
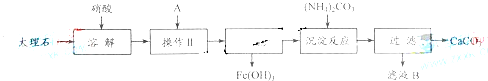
(2009?上海)实验室用大理石等原料制取安全无毒的杀菌剂过氧化钙.大理石的主要杂质是氧化铁.以下是提纯大理石的实验步骤:
(1)溶解大理石时,用硝酸而不用硫酸的原因是
硫酸钙微溶于水
硫酸钙微溶于水
.
(2)操作Ⅱ的目的是
除去溶液中Fe3+
除去溶液中Fe3+
,溶液A(溶质是共价化合物)是
氨水
氨水
.
(3)写出检验滤液中是否含铁离子的方法:
取少量滤液,向其中加入硫氰化钾溶液,溶液不变红色,说明滤液中不含Fe3+;
或取少量滤液,向其中加入硫氰化钾溶液,溶液变红色,说明滤液中含Fe3+
取少量滤液,向其中加入硫氰化钾溶液,溶液不变红色,说明滤液中不含Fe3+;
或取少量滤液,向其中加入硫氰化钾溶液,溶液变红色,说明滤液中含Fe3+
.
(4)写出加入碳酸铵所发生反应的离子方程式:
Ca2++CO32-═CaCO3↓
Ca2++CO32-═CaCO3↓
写出滤液B的一种用途:
作化肥
作化肥
.
(5)CaO
2中一般含CaO.试按下列提示完成CaO
2含量分析的实验设计.
试剂:氢氧化钠标准溶液、盐酸标准溶液、酚酞仪器:电子天平、锥形瓶、滴定管
实验步骤:
①
称量
称量
;②加入
过量的标准盐酸
过量的标准盐酸
;③加入酚酞,用氢氧化钠标准溶液滴定.
(6)若理论上滴定时耗用标准溶液20.00mL恰好完全反应,实际操作中过量半滴(1mL溶液为25滴),则相对误差为
0.1%
0.1%
.