
| A. | 蒸馏、分馏、干馏都属于物理变化 | |
| B. | 石油裂解可以得到氯乙烯 | |
| C. | 油脂水解可得到氨基酸和甘油 | |
| D. | 淀粉和纤维素的组成都是(C6H10O5)n,水解最终产物都是葡萄糖 |
分析 A.没有新物质生成的变化是物理变化,有新物质生成的变化是化学变化;
B.石油裂解的目的是获得乙烯;
C.油脂是高级脂肪酸甘油酯;
D.淀粉和纤维素的组成都是(C6H10O5)n.
解答 解:A.利用原油中各组分沸点的不同进行分离的过程叫分馏,属于物理变化,故A错误;
B.石油裂解是使具有长链分子的烃断裂成各种短链的气态烃和少量液态烃,以提供有机化工原料.石油裂解得到的为小分子的烃类,故B错误;
C.油脂是高级脂肪酸甘油酯,水解得到高级脂肪酸和甘油,故C错误;
D.淀粉和纤维素水解的最终产物都是葡萄糖,故D正确.
故选D.
点评 本题考查石油的分馏产品、糖类油脂的性质、同分异构体等,难度不大,注意乙烯是通过石油的裂解获得.


科目:高中化学 来源: 题型:选择题
| A. | 950mL,111.2g | B. | 1000 mL,117.0g | C. | 500mL,117g | D. | 任意规格,111.2g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钾的原子质量就是钾的相对原子质量 | |
| B. | 一个硫原子的实际质量约等于$\frac{32}{(6.02×1{0}^{23})}$g | |
| C. | 水的相对分子质量为18g | |
| D. | 17g OH-中所含电子数为9NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
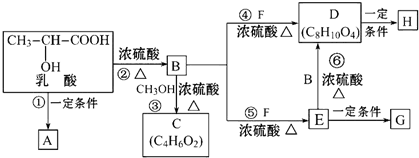
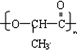 ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子晶体中每个离子周围均吸引着6个带相反电荷的离子 | |
| B. | 在晶体中,若有阳离子一定存在阴离子 | |
| C. | 分子晶体中一定不含有离子键,但一定存在共价键 | |
| D. | 原子晶体中的各相邻原子都以共价键结合 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由乙烯与氧气在Ag作催化剂下反应制取环氧乙烷原子利用率可达100% | |
| B. | 高聚物的相对分子质量一定为单体相对分子质量的整数倍 | |
| C. |  分子中只存在羧基、羟基两种官能团 分子中只存在羧基、羟基两种官能团 | |
| D. |  分子中至少有14个原子共平面 分子中至少有14个原子共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
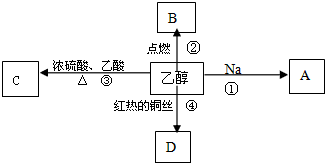
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 按要求完成硝酸钾晶体的制备实验:
按要求完成硝酸钾晶体的制备实验:| 步骤 | 操作 | 具体操作步骤 | 现象解释结论等 |
① | 溶解 | 取20克KNO3和17克NaCl溶解在35ml水中,加热至沸,并不断搅拌. | 固体溶解 |
| ② | 蒸发 | 继续加热搅拌,使溶液蒸发浓缩. | 有a晶体析出. |
| ③ | 热过滤 | 当溶液体积减少到约原来的一半时,迅速趁热过滤 | 滤液中的最主要成分为b. |
| ④ | 冷却 | 将滤液冷却至室温. | 有晶体析出. |
| ⑤ | 按有关要求进行操作 | 得到初产品硝酸钾晶体 | |
⑥ | 将得到的初产品硝酸钾晶体溶于适量的水中,加热、搅拌,待全部溶解后停止加热,使溶液冷却至室温后抽滤. | 得到纯度较高的硝酸钾晶体 | |
| ⑦ | 检验 | 分别取⑤、⑥得到的产品,配置成溶液后分别加入1滴1mol/l的HNO3和2滴0.1mol/l的AgNO3 | 可观察到⑤、⑥产品中出现的现象分别是⑤产品中产生白色沉淀,⑥产品中无明显现象. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化铁在高温下与一氧化碳反应 | |
| B. | 二氧化碳与氢氧化钠溶液作用生成碳酸钠 | |
| C. | Zn 粒与稀硫酸反应制取氢气 | |
| D. | 碳酸钠溶液与石灰乳混合 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com