
已知锌溶于稀硝酸中可发生如下反应:4Zn+10HNO3==4Zn(NO3)2+N2O↑+5H2O,该反应中被还原的硝酸与未被还原的硝酸的质量比是
A.2∶5 B.1∶4 C.4∶1 D.5∶1
B
【解析】
试题分析:此反应中元素的化合价变化情况为: 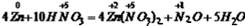 ,即参加反应的10个HNO3中的+5价N,反应生成了4个Zn(NO3)2中+5价的N,即化合价未发生变化,又生成了1个N2O中的+1价的N,化合价降低被还原,故从生成的4个Zn(NO3)2中可看出有8各+5价N未变化,生成1各N2O中有2个+5价生成了2个+1价的N,故被还原的HNO3是2,即得被还原的HNO3和未被还原的HNO3的个数比是2:8,即1:4,因此得被i还原的HNO3和未被还原的HNO3的质量比是:(1*63):(4*63)=1:4。
,即参加反应的10个HNO3中的+5价N,反应生成了4个Zn(NO3)2中+5价的N,即化合价未发生变化,又生成了1个N2O中的+1价的N,化合价降低被还原,故从生成的4个Zn(NO3)2中可看出有8各+5价N未变化,生成1各N2O中有2个+5价生成了2个+1价的N,故被还原的HNO3是2,即得被还原的HNO3和未被还原的HNO3的个数比是2:8,即1:4,因此得被i还原的HNO3和未被还原的HNO3的质量比是:(1*63):(4*63)=1:4。
故选B。
考点:硝酸
点评:本题考查的是有关硝酸的氧化性的相关知识,解答此题需要学生能正确的分析出化学反应中元素化合价的变化情况。


科目:高中化学 来源: 题型:
| A、2:5 | B、1:4 | C、4:1 | D、5:1 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年山西省忻州一中高一上学期期末联考化学试卷(A)(带解析) 题型:单选题
已知锌溶于稀硝酸中可发生如下反应:4Zn+10HNO3==4Zn(NO3)2+N2O↑+5H2O,该反应中被还原的硝酸与未被还原的硝酸的质量比是
| A.2∶5 | B.1∶4 | C.4∶1 | D.5∶1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:
以下框图是无机物A ~ N的转化关系(部分产物及反应条件未列出)。已知E、F、G、J为单质,且E、F为金属单质;物质M、M′由相同元素组成,M′是黄色固体,M′常用于工业上制取A;D、I也由相同元素组成,I为黑色有磁性的晶体;B是有臭鸡蛋气味的气体,C是有刺激性气味的气体。请根据以上框图填写以下空白:

(1)B的电子式是______________;
B分子属_________分子(填“极性”或“非极性”);
(2)B与C气体间反应的实验现象是
;
将E或F金属片放入A的浓溶液中,现象是___________ ____________________;
(3)用石墨作电极,以碱性锌锰干电池电解H,己知干电池总反应为:Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,阳极的电极反应式是 。当生成J的气体体积为11.2L(标准状况)时,干电池消耗的负极材料质量为 g;
(4)C与N溶液反应的离子方程式是 ;
I溶于稀硝酸的离子反应方程式为 ;
(5)过量F溶于HI的溶液,取所得溶液再与过量稀HNO3反应的离子反应方程式为:
;
(6)在化工生产中,由M′制A,现有100T质量分数为80℅的M′参加反应,若几步反应总的转化率为80℅,则可生成98℅的A溶液 T(结果保留一位小数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com