
| A. | NH3 | B. | O2 | C. | H2O | D. | CO2 |
分析 发生反应NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑,过氧化钠与二氧化碳、水反应生成氧气,浓硫酸可以吸收氨气,据此解答.
解答 解:发生反应NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑,放出的气体通过盛有足量过氧化钠的干燥管,过氧化钠与二氧化碳、水反应生成氧气,从盛放过氧化钠的干燥管出来气体为氨气、氧气,在通过足量浓H2SO4 的洗气瓶,浓硫酸稀释氨气,最后得到的气体为氧气,故选B.
点评 本题考查铵盐与过氧化钠等性质、物质推断等,难度不大,掌握物质的性质是关键.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐酸浓度不变,使用量增大1倍 | B. | 盐酸浓度增加1倍,但用量减至1/2 | ||
| C. | 将碳酸钙固体改为碳酸钙粉末 | D. | 加热此反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
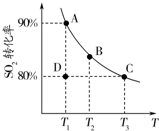 研究硫及其化合物性质有重要意义.
研究硫及其化合物性质有重要意义.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在混合物中加入足量浓硫酸,加热、过滤 | |
| B. | 在混合物中加入足量NaOH溶液,过滤 | |
| C. | 用磁石将铁粉吸出 | |
| D. | 在混合物中加入足量浓硝酸,加热、过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2mol | B. | 3mol | C. | 1.5mol | D. | 0.2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某气体能使品红溶液褪色,则该气体是SO2 | |
| B. | 向某溶液中加入AgNO3溶液,产生白色沉淀,则原溶液中有Cl- | |
| C. | 某溶液中加入稀盐酸,不产生白色沉淀,再加入BaCl2溶液,产生白色沉淀,原溶液中有SO42- | |
| D. | 某溶液中加入盐酸产生无色气体,且该气体能使澄清石灰水变浑浊,则原溶液中一定含有CO32-或者HCO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com