
【题目】某课外小组的同学拟用废铝箔制取硫酸铝晶体,已知铝的物种类别与溶液pH关系如图所示.
实验中可选用的试剂:①处理过的铝箔;②2.0molL﹣1硫酸;③2.0molL﹣1NaOH溶液.
由铝箔制备硫酸铝晶体的实验步骤依次为:
①称取一定质量的铝箔于烧杯中,分次加入2.0molL﹣1NaOH溶液,加热至不再产生气泡为止.
②过滤.
③ .
④过滤、洗涤.
⑤ .
⑥蒸发浓缩.
⑦冷却结晶.
⑧过滤、洗涤、干燥.
【答案】滤液中滴加2.0mol?L﹣1硫酸,不断搅拌,调节溶液pH为4~10;沉淀中不断加入2.0mol?L﹣1硫酸至恰好溶解
【解析】解:铝与氢氧化钠反应生成偏铝酸钠与氢气,过滤,向滤液中加入硫酸,由图可知,调节pH在4﹣10时生成氢氧化铝沉淀,再过滤、洗涤,向沉淀中加入稀硫酸,至恰好溶解,从溶液中获得晶体,需要蒸发浓缩、冷却结晶,再进行过滤、洗涤、干燥得到硫酸铝晶体.③根据图片知,pH在4~10时生成氢氧化铝沉淀,所以该步骤是:向滤液中滴加2.0molL﹣1硫酸,不断搅拌,调节溶液pH为4~10,从而得到氢氧化铝沉淀,
所以答案是:滤液中滴加2.0molL﹣1硫酸,不断搅拌,调节溶液pH为4~10;⑤该实验目的是制取硫酸铝晶体,所以用得到的氢氧化铝沉淀制取硫酸铝溶液,其操作方法是:沉淀中不断加入2.0molL﹣1硫酸至恰好溶解,所以答案是:沉淀中不断加入2.0molL﹣1硫酸至恰好溶解.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列离子检验的方法正确的是( )
A.某溶液加入硝酸银溶液有白色沉淀,说明原溶液中有Cl﹣
B.某溶液加入氯化钡溶液有白色沉淀,说明原溶液中有SO ![]()
C.某溶液加入氢氧化钠溶液有蓝色沉淀,说明原溶液中有Cu2+
D.某溶液加入稀硫酸生成无色气体,说明原溶液中有CO ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各物质的转化关系如下图所示,A是一种高熔点金属氧化物,D是一种红棕色固体.
回答下列问题:
(1)填写下列物质的化学式:A;B;D;H .
(2)写出下列反应的方程式:①C+D→A+E的化学方程式: .
②A→H的离子方程式: .
③F→G的化学方程式:、 .
(3)F→G反应现象: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环己酮是重要化工原料,是制造尼龙、己内酰胺和己二酸的主要中间体.实验室常用铬酸氧化环己醇制备,但铬酸较贵且污染环境.某化学兴趣兴趣小组尝试用中学化学更常见的次氯酸钠代替铬酸制备环己酮.有关物质信息、实验流程如图1及实验装置如图2如下:环己酮:无色或浅黄色透明液体,有强烈的刺激性臭味,相对水的密度:0.95,熔点:﹣45℃,沸点:155℃,溶解度(100mL H2O):2.4g (31℃ ). 回答下列问题:
回答下列问题:
(1)仪器A的名称是 .
(2)在反应开始的5min,为了将体系温度维持在30~35℃,除了用冰水浴冷却外,采取的措施还有、 .
(3)加入饱和NaHSO3溶液时发生的主要反应是(用离子方程式表示),确保加入的饱和NaHSO3溶液已经足量的实验操作是 .
(4)为将馏出液的pH调至中性,可以加入的试剂是 .
A.稀盐酸
B.无水碳酸钠
C.浓硫酸
D.氢氧化钠固体
(5)调节pH后还需加入精制食盐,其目的是 , “取有机层”时使用的主要仪器是 . (填图3对应的字母).
(6)实验条件的优化对实验成败至关重要,小组成员觉得有必要对NaClO溶液的最佳浓度进行探究.他们配制了一系列不同浓度的NaClO溶液,并用滴定法标定.具体方法是:用移液管取10.00mL NaClO溶液于500mL容量瓶中定容,取25.00mL于锥形瓶中,加入适量稀盐酸和KI固体(足量),用0.1000mol/L Na2S2O3标准溶液滴定至终点(用淀粉溶液作指示剂),三次平行实验平均消耗Na2S2O3标准溶液18.00mL,已知I2+2Na2S2O3═2NaI+Na2S4O6 . 则该NaClO溶液的浓度是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物J具有抗缺血性脑损伤的作用,合成J的一种路线如图: 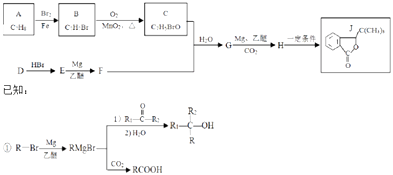
②E的核磁共振氢谱只有一组峰
③C能发生银镜反应
回答下列问题:
(1)D所含有官能团的名称 .
(2)由D生成E的化学方程式为 , 其反应类型为 .
(3)G的结构简式为 .
(4)C的某同系物X,相对分子质量比C大14,X的结构有种,其中核磁共振氢谱为4组峰,且锋面积比为1:2:2:2的是(写结构简式).
(5)由甲醛和化合物A经下列步骤可得到2﹣苯基乙醇. ![]()
反应条件1为;反应条件2所选择的试剂为;L的结构简式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】冰箱制冷剂氟氯甲烷在高空受紫外线辐射时产生Cl·原子,并能发生下列反应:Cl·+O3―→ClO·+O2 , ClO·+O·―→Cl·+O2。下列说法不正确的是( )
A.反应过程中将O3转变为O2
B.Cl是总反应的催化剂
C.氟氯甲烷是总反应的催化剂
D.Cl起分解O3的作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.由徐光宪院士发起,院士学子同创的《分子共和国》科普读物最近出版了,全书形象生动地戏说了BF3、TiO2、CH3COOH、CO2、NO、二茂铁、NH3、HCN、H2S、O3、异戊二烯和萜等众多“分子共和国”中的明星.
(1)写出Fe2+的核外电子排布式 .
(2)下列说法正确的是 .
a.H2S、O3分子都是直线形
b.BF3和NH3都是含有极性键的非极性分子
c.CO2、HCN分子的结构式分别是:O=C=O、H﹣C≡N
d.CH3COOH分子中碳原子的杂化方式有:sp2、sp3
(3)NO是人体中的信号分子,有关说法正确的 .
a.原子半径N大于O b.非金属性O大于N
c.NO+的结构式为:〔N≡O〕+ d.NO形成的晶体是分子晶体
(4)TiO2的天然晶体中,最稳定的一种晶体结构如图1,白球表示原子.
(5)乙酸熔沸点很高,是由于存在以分子间氢键缔合的二聚体(含一个环状结构),请画出这二聚体的结构: .
(6)二茂铁(C5H5)2Fe是Fe2+与环戊二烯基形成的一类配合
物,实验室测定铁的含量:可用配位剂邻二氮菲
( ![]() ),它能与Fe2+形成红色配合物(如右图2),
),它能与Fe2+形成红色配合物(如右图2),
该配离子中Fe2+与氮原子形成配位键共有个.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质或应用的说法正确的是
A. 医疗上,常用碳酸钠治疗胃酸过多
B. 在海轮外壳上安装锌块以减缓船体腐蚀
C. 液氨汽化放出大量的热,可用作制冷剂
D. 明矾具有强氧化性,常用于自来水的杀菌消毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上产生的氮氧化物可用天然气来处理.
(1)Ⅰ.已知:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H1
N2(g)+2O2(g)=2NO2(g)△H2
H2O(l)=H2O(g)△H3
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△ H=(用△ H1、△ H2、△ H3)
(2)Ⅱ.在温度为T1℃和T2℃时,分别将0.50molCH4和1.2molNO2充入体积固定的2L密闭容器中,发生上述可逆反应,测得不同时刻的n(CH4)数据如下表:
温度 | 时间/min | 0 | 10 | 20 | 40 | 50 |
T1℃ | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2℃ | n(CH4) | 0.50 | 0.30 | 0.18 | 0.15 | 0.15 |
①分析上表中数据,下列说法正确的是
A.T1℃ 前10min,V(NO2)=0.03mol/(Lmin)
B.T1℃ 反应达化学平衡状态时,CH4的转化率为80%
C.T2℃ 反应在40min时处于平衡状态
D.T1>T2
②反应的平衡常数K(T1) K(T2),△H0,理由是 .
③T1℃时反应的平衡常数K为 .
④反应在T1℃下进行,50min时,向平衡后的容器中再通入0.10molCH4和0.40molNO2 , 在下图中画出恒温,重新达到平衡过程中n(CH4)随时间变化的曲线(只要求画出n(CH4)的变化趋势,不需要准确画出再次平衡后n(CH4) .
(3)Ⅲ.NO2、O2和熔融NaNO3可制作燃料电池,其原理见下图.该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,其电极反应式为 . 
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com