
【题目】下列反应既是氧化还原反应,又是吸热反应的是( )
A. 灼热的炭与CO2反应 B. Ba(OH)2·8H2O与NH4Cl反应
C. 铝片与稀H2SO4反应 D. 甲烷在O2中的燃烧反应
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案科目:高中化学 来源: 题型:
【题目】谢弗勒尔盐(Cu2SO3·CuSO3·2H2O)是一种不溶于水、酸和乙醇的固体,100℃时发生分解。可由CuSO4·5H2O和SO2等为原料制备,实验装罝如下图所示:
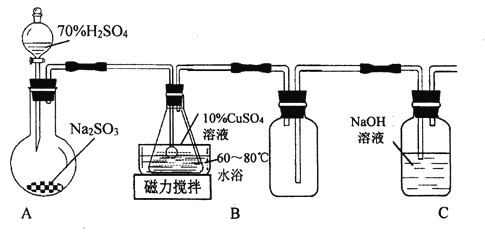
(1)装置A在常温下制取SO2时,用70%硫酸而不用稀硫酸和98%浓硫酸,其原因是________。
(2)装置B中发生反应的离子方程式为_________。
(3)装置C的作用是__________。
(4)从B中获得的固体需先用蒸馏水充分洗涤,再真空干燥。检验己洗涤完全的方法是________________。
(5)请补充完整由工业级氧化铜(含少量FeO)制备实验原料(纯净CuSO4·5H2O) 的实验方案:向工业级氧化铜中边搅拌边加入稍过量的硫酸溶液,微热使其完全溶解,边搅拌边向其中滴入______溶液,加入适最纯净的________调节3.2<pH<4.2,静置,过滤,将滤液水浴加热蒸发浓缩至表面出现晶膜,冷却结晶,过滤,用95% 酒精洗涤晶体2~3次,晾干,得到CuSO4·5H2O。
[已知:该溶液中氢氧化物开始沉淀与沉淀完全时的pH范围分别为:Fe(OH)2 (5.8, 8.8); Cu(OH)2 (4.2, 6.7); Fe(OH)3 (1.1,3.2)]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1mol乙醇(其中的氧用18O标记)在浓硫酸存在并加热下与足量乙酸充分反应.下列叙述正确的是( )
A.水分子中含有18OB.乙酸乙酯中含有18O
C.最终体系中四种分子中都含有18OD.生成90g乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中,正确的是
A.Fe片投入浓硫酸中:Fe+2H+→ Fe2++H2↑
B.硫酸铝溶液滴入过量烧碱溶液中:Al3++4OH-→ AlO2-+ 2H2O
C.FeS放入稀盐酸溶液中:S2-+2H+ →H2S↑
D.在AlCl3溶液中加入过量氨水:Al3++4NH3·H2O→ AlO2-+4NH4++2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一容积为2L的密团容器内加入0.2molN2和0.6molH2,在一定条件下发生如下反应: ![]() N2(g)+
N2(g)+ ![]() H2(g)
H2(g)![]() NH3(g)
NH3(g)
①该反应的平衡常数的表达式是:____________。
②反应中氨气的浓度的变化情况如图所示,计算从反应开始到平衡时,平均反应速率v(H2)=________。
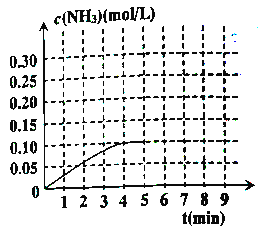
③判断该反应达到平衡状态的标志是_________。
a.N2和NH3浓度相等 b.NH3百分含量保持不变
c.容器中气体的压强保持不变 d.NH3的生成速率与H2的消耗速率相等
e.容器中混合气体的密度保持不变
④反应达平衡后,第5分钟末,保持其它条件不变,仅改变反应温度,则NH3的物质的量浓度不可能为______。
a.0.2mol/L b.0.12mol/L c.0.10mol/L d.0.08mol/L
⑤在第5分钟末,将容器体积缩小一半后,若在第8分钟末达到新平衡(此时NH3浓度约为0.25mol/L),请在上图中画出从第5分钟末开始,再达到新平衡时NH3浓度变化曲线。______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
选项 | 实验 | 现象 | 结论 |
A | 用pH试纸检测:0.1 mol·L1 Na2SO3溶液、0.1 mol·L1 NaHSO3溶液 | Na2SO3溶液的pH约为10;NaHSO3溶液的pH约为5 |
|
B | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体 | 溶液红色变浅 | Na2CO3溶液中存在水解平衡 |
C | 注射器中吸入NO2,封堵针尖处,将注射器体积压缩为原来的一半 | 气体颜色比起始时浅 | 加压后,NO2转变为无色的N2O4 |
D | 饱和BaSO4悬浊液中加入饱和Na2CO3溶液,振荡,然后过滤、洗涤,向所得固体中加入盐酸 | 沉淀部分溶解且有气体产生 | Ksp(BaSO4) > Ksp(BaCO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】20种氨基酸的平均相对分子质量为128,假若有一个多肽化合物,由10个氨基酸构成一个肽链,那么该多肽的相对分子质量和至少含有的氨基数目分别是 ( )
A. 1 280,11 B. 1 262,1 C. 1 118,1 D. 1 100,9
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LiAlH4( )、LiH既是金属储氢材料又是有机合成中的常用试剂,遇水均能剧烈分解释放出H2,LiAlH4在125℃分解为LiH、H2和Al。下列说法不正确的是
)、LiH既是金属储氢材料又是有机合成中的常用试剂,遇水均能剧烈分解释放出H2,LiAlH4在125℃分解为LiH、H2和Al。下列说法不正确的是
A.LiH与D2O反应,所得氢气的摩尔质量为4 g/mol
B.1 mol LiAlH4在125℃完全分解,转移3 mol电子
C.LiAlH4溶于适量水得到无色溶液,则化学方程式可表示为:LiAlH4 + 2H2O![]() LiAlO2 + 4H2↑
LiAlO2 + 4H2↑
D.LiAlH4与乙醛作用生成乙醇,LiAlH4作还原剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com