
【题目】根据下列提供的一组物质回答问题:
①NH4Cl ②MgCl2 ③H2S ④Na2O2 ⑤MgO ⑥Cl2 ⑦NaOH
(1)仅含有共价键的是_________;既有离子键又有共价键的是_________(用序号表示)
(2)离子化合物有_____________________;(用序号表示)
(3)Na2O2 的电子式_____________________
【答案】③⑥ ①④⑦ ①②④⑤⑦ ![]()
【解析】
(1)离子键是阴阳离子间的静电作用,共价键是原子间通过共用电子对形成的相互作用;
(2)含有离子键的化合物属于离子化合物;
(3)过氧化钠是由2个钠离子与1个过氧根离子通过离子键结合而成的离子化合物。
(1)①NH4Cl,含有离子键和共价键;
②MgCl2含有离子键;
③H2S只含有共价键;
④Na2O2含有离子键和共价键;
⑤MgO含有离子键;
⑥Cl2只含有共价键;
⑦NaOH,含有离子键和共价键;
仅含共价键的是:③⑥;既有离子键又有共价键的是①④⑦;
故答案为:③⑥;①④⑦。
(2)含有离子键的化合物有:①②④⑤⑦,属于离子化合物;故答案为:①②④⑤⑦。
(3)过氧化钠是由2个钠离子与1个过氧根离子通过离子键结合而成的离子化合物,电子式为:![]() ,故答案为:
,故答案为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】下列关于氧化物的叙述正确的是( )
A.非金属氧化物一定是酸性氧化物B.碱性氧化物一定是金属氧化物
C.酸性氧化物一定是非金属氧化物D.碱性氧化物都能与水化合生成碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质的用途,叙述不正确的是
A.二氧化硫可广泛用于食品的增白B.Na2SiO3常用作制木材防火剂
C.硅胶可用作食品干燥剂D.硅可用于制作硅芯片和光电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的原电池装置,X、Y为两电极,电解质溶液为稀硫酸,外电路中的电子流向如图所示,对此装置的下列说法正确的是( )

A. 外电路的电流方向为:X→外电路→Y
B. 若两电极分别为Zn和石墨棒,则X为石墨棒,Y为Zn
C. SO42-移向X电极,Y电极上有氢气产生
D. X极上发生的是还原反应,Y极上发生的是氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科研小组利用甲醇燃料电池进行如下电解实验,其中甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O,下列说法不正确的是

A. 甲池中通入CH3OH的电极反应:CH3OH-6e-+8OH-=CO32-+6H2O
B. 甲池中消耗560mLO2(标准状况下),理上乙池Ag电极增重3.2g
C. 反应一段时间后,向乙池中加入一定量Cu(OH)2固体,能使CuSO4溶液恢复到原浓度
D. 丙池右侧Pt电极的电极反应式:Mg2++2H2O+2e-=Mg(OH)2↓+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CaC2晶体的晶胞结构与NaCl晶体的相似(如图所示),但CaC2晶体中由于哑铃形的C22-存在,使晶胞沿一个方向拉长。下列关于CaC2晶体的说法中正确的是
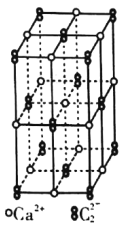
A. CaC2晶体中,所有原子之间都以离子键相结合
B. C22-与N2互为等电子体
C. 1个Ca2+周围距离最近且等距离的C22-数目为6
D. 1个CaC2晶体的晶胞平均含有1个Ca2+和1个C22-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子。使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ·mol-1表示。请认真观察下图,然后回答问题。
(1)下图中所示反应是________(填“吸热”或“放热”)反应。

(2)已知拆开1mol H—H键、1mol I—I、1mol H—I键分别需要吸收的能量为436kJ、151kJ、299kJ。则由1mol氢气和1mol 碘反应生成HI会____(填“放出”或“吸收”)____kJ的热量。
(3)下列反应中,属于放热反应的是________,属于吸热反应的是________。
①物质燃烧 ②炸药爆炸 ③酸碱中和反应 ④二氧化碳通过炽热的碳
⑤食物因氧化而腐败 ⑥Ba(OH)2·8H2O与NH4Cl反应 ⑦铁粉与稀盐酸反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
A. 1L1.0mo1L-1的NaAlO2水溶液中含有的氧原子数为2NA
B. 标准状况下,11.2LNO与11.2LO2混合后所含分子数为0.75NA
C. Na2O和Na2O2混合物的物质的量为1mol,其中含有的阴离子总数为NA
D. 室温下,将9g铝片投入0.5L 18.4molL-1的H2SO4中,转移的电子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题目要求,回答下列问题。
(1)选择下面的实验装置完成相应的实验:

实验室制取乙烯用到的装置是_____________(填写序号,下同);分离苯和甲苯用到的装置是__________________;提纯苯甲酸过程中进行分离操作用到的装置是__________________;用CCl4萃取溴水中的溴用到的装置是__________________;
(2)以下是五种常见有机物分子模型示意图,其中A、B、C为烃,D、E为烃的含氧衍生物。

鉴别A和B的试剂为__________________;上述物质中有毒、有特殊气味,且不溶于水、密度比水小的液体是____________(填名称);D分子中的官能团的结构简式是_______________;检验E中的官能团可以选用的试剂是______________________。
(3)写出下列化学方程式:
 与足量溴水反应_____________________________________;
与足量溴水反应_____________________________________; 与足量NaOH溶液反应_____________________________________。
与足量NaOH溶液反应_____________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com