
将反应4(NH4)2SO4→N2↑+6NH3↑+3SO2↑+SO3↑+7H2O的产物气体通入BaCl2溶液,下列判断正确的是( )
|
| A. | 无沉淀生成 |
|
| B. | 得到的沉淀是BaSO4和BaSO3组成的混合物 |
|
| C. | 得到的沉淀是纯净物 |
|
| D. | 肯定没有BaSO3生成 |
| 氧化还原反应. | |
| 分析: | 二氧化硫溶于水和水反应生成亚硫酸,三氧化硫溶于水和水反应生成硫酸,氨气溶于水生成一水合氨;硫酸和氯化钡反应生成硫酸钡沉淀,亚硫酸和氨水反应生成亚硫酸铵,所以通入氯化钡溶液中,生成沉淀有亚硫酸钡和硫酸钡,以此来解答. |
| 解答: | 解:硫酸铵分解反应为4(NH4)2SO4=N2↑+6NH3↑+3SO2↑+SO3↑+7H2O,反应后的混合气体通入到BaCL2溶液中发生的是复分解反应, SO2+H2O+2NH3=(NH4)2SO3 、(NH4)2SO3+BaCl2=BaSO3↓+2NH4Cl、SO3+H2O+2NH3 =(NH4)2SO4、(NH4)2SO4+BaCl2=BaSO4↓+2NH4Cl, 由反应可知,设4mol(NH4)2SO4分解,生成1molN2,6molNH3,3molSO2,1molSO3, 二氧化硫转化为亚硫酸铵,1mol三氧化硫转化为硫酸铵消耗氨气2mol,则4mol氨水和2mol二氧化硫反应生成2mol亚硫酸铵, 所以得到的沉淀为1mol硫酸钡,2mol亚硫酸钡,剩余二氧化硫和亚硫酸钡反应生成亚硫酸氢钡, 最后得到沉淀为1mol硫酸钡,1mol亚硫酸钡, 因此得到沉淀为BaSO3和BaSO4, 故选B. |
| 点评: | 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应分析及应用能力的考查,题目难度不大. |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
天然维生素P(结构简式如图)存在于槐树花蕾中,它是一种营养增补剂,关于维生素P的叙述错误的是

A.可以和溴水反应
B.可用有机溶剂萃取
C.分子中有三个苯环
D.1 mol维生素P可以和4 mol NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与生活是紧密相联的,下列说法正确的是
A.为防止中秋月饼等富脂食品氧化变质,常在包装袋中放入生石灰
B.海水淡化能解决淡水供应危机,向海水中加净水剂明矾可以使海水淡化
C.为了增强漂白粉的使用效果,在使用漂白粉时必须和盐酸混合使用
D.今年春天,在我国南方发生了不同程度的旱情,缓解旱情的措施之一是可以用干冰或碘化银进行人工降雨
查看答案和解析>>
科目:高中化学 来源: 题型:
某品牌糖衣片补血剂,除去糖衣后显淡蓝绿色,主要成分是硫酸亚铁,不含其它铁的化合物。某研究性学习小组为测定该补血剂中硫酸亚铁的含量进行了以下探究:
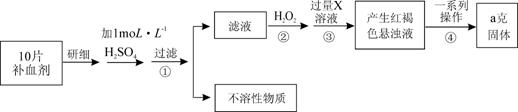 |
请回答下列问题:
Ⅰ.(1)实验时用18.4 mol·L-1的浓硫酸,配制100 mL 1 mol·L-1 H2SO4溶液,所需浓硫酸的体积为 。(计算结果精确到小数点后一位)
(2)下列操作中,容量瓶所具备的功能有 (填序号)。
A.配制一定体积准确浓度的标准溶液 B.长期贮存溶液
C.用来溶解固体溶质 D.常用来代替量筒量取一定体积的液体
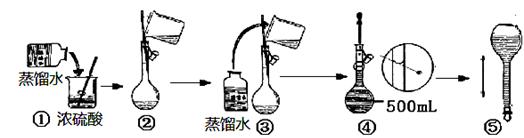 (3)在下列配制过程示意图中,有错误的是(填写序号) 。
(3)在下列配制过程示意图中,有错误的是(填写序号) 。
 | |||||
| |||||
|
(4)下列说法正确的
A.洗涤烧杯2~3次,并将洗涤液移入容量瓶以减少误差
B.某同学将浓硫酸稀释后未冷却至室温便将溶液转移至容量瓶,所配溶液浓度会偏低
C.定容时仰视观察, 所配溶液浓度会偏低
D.容量瓶使用前先要检查是否漏液,具体操作是向容量瓶中加蒸馏水,倒置不漏液即可
Ⅱ.(1)步骤②加入过量H2O2的目的: 。
(2)从红褐色的悬浊液到最后的称量,其过程中所需的基本操作为:
a. ,b. 洗涤,c. 灼烧,d. 冷却
(3)若称得固体的质量为ag,则每片补血剂中含硫酸亚铁的质量为 。
Ⅲ.已知人体不能很好地吸收利用Fe3+,科学研究表明服用含硫酸亚铁的补血剂时,同时服用维生素C,以利于铁元素的吸收。试分析维生素C在这一过程中的作用是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
一容器中X元素构成的气态单质X2分子有3种,相对分子质量分别为32、34、36.又知容器中3种分子数之比为15:4:1.由此可以确定的是( )
|
| A. | 若容器中X2全部转化为它的同素异形体X3,那么X3的分子量有3种 |
|
| B. | 质量数为16的一种核素在此容器中的原子百分数为85% |
|
| C. | 只要容器中同位素组成不变,X原子在任何条件下发生重新组合,最后得到三种 X2,分子数之比总是15:4:1 |
|
| D. | 此容器中X2的平均分子量是34 |
查看答案和解析>>
科目:高中化学 来源: 题型:
将几滴KSCN(SCN﹣是“类卤离子”,与氯离子性质相似)溶液加入酸性的含有Fe3+的溶液中,溶液变成血红色.将该红色溶液分为两份,①一份中加入适量KMnO4溶液,红色褪去;②向另一份中通入SO2,红色也褪去.下列说法不正确的是( )
|
| A. | ①红色褪去的原因可能是KMnO4将SCN﹣氧化,使[Fe(SCN)]2+消失 |
|
| B. | [Fe(SCN)]2+中Fe3+与SCN﹣以配位键结合 |
|
| C. | ②红色褪去的原因是SO2具有还原性 |
|
| D. | SCN﹣在适当条件下可被还原为(SCN)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
将一定量的氯气通入30mL浓度为10.00mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系.下列判断正确的是( )
|
| A. | 与NaOH反应的氯气一定为0.3 mol |
|
| B. | n(Na+):n(Cl﹣)可能为7:3 |
|
| C. | 若反应中转移的电子为n mol,则0.15<n<0.25 |
|
| D. | n(NaCl):n(NaClO):n(NaClO3)可能为11:2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图在试管Ⅰ中先加入3mL 95%的乙醇, 并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2mL无水乙酸,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管Ⅱ中加入5ml 饱和的碳酸钠溶液,按图连接好装置,用酒精灯对试管Ⅰ小火加热3~5min后,改用大火加热,当观察到试管Ⅰ中有明显现象时停止加热。试回答:
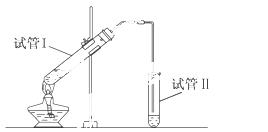
(1)试管Ⅱ中的导管不插入液面下的原因是 ;
(2)反应完毕后,振荡试管Ⅱ,观察到试管Ⅱ中的现象是 ;
(3)试管Ⅰ中加入浓硫酸的作用是 ;
(4)本实验反应开始时用小火加热的原因是 ________;(已知乙酸乙酯的沸点为77℃;乙醇的沸点为78.5℃;乙酸的沸点为117.9℃)
________;(已知乙酸乙酯的沸点为77℃;乙醇的沸点为78.5℃;乙酸的沸点为117.9℃)
(5)试管Ⅱ中饱和Na2 CO3的作用是
CO3的作用是
(6)写出试管Ⅰ中发生反应的化学方程式 
该反应的反应类型是
查看答案和解析>>
科目:高中化学 来源: 题型:
利用实验器材(规格和数量不限)能完成相应实验的一项是
| 选项 | 实验器材(省略夹持装置) | 相应实验 |
| A | 烧杯、玻璃棒、蒸发皿 | CuSO4溶液的浓缩结晶 |
| B | 烧杯、玻璃棒、胶头滴管、滤纸 | 用盐酸除去BaSO4中的少量BaCO3 |
| C | 烧杯、玻璃棒、胶头滴管、容量瓶 | 用固体NaCl配制0.5mol/L的溶液 |
| D | 烧杯、玻璃棒、胶头滴管、分液漏斗 | 用溴水和CCl4除去NaBr溶液中的少量NaI |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com