
与Cl2相比较,ClO2处理水时被还原成Cl-,不生成有机氯代物等有害物质。工业上可用亚氯酸钠和稀盐酸为原料制备ClO2,反应如下:
NaClO2+HCl—→ClO2↑+________(没有配平)
(1)上述方程式中,缺项物质是________,配平方程式,并在下面补全反应物系数。
 NaClO2+
NaClO2+ HCl—→
HCl—→
(2)该反应中氧化剂和还原剂的物质的量之比是________________________。
生成0.2 mol ClO2转移电子的物质的量为________ mol。
(3)ClO2对污水中的Fe2+、Mn2+、S2-和CN-等有明显的去除效果。某污水中含CN- a mg·L-1,现用ClO2将CN-氧化,只生成两种无毒气体。处理100 m3这种污水,至少需要ClO2________ mol。
科目:高中化学 来源: 题型:
物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度等有关。下列各组物质:①Cu与HNO3溶液 ②Cu与FeCl3溶液 ③Zn与H2SO4溶液 ④Fe与FeCl3溶液 ⑤Cl2和NaOH溶液 ⑥Fe和HNO3溶液 ⑦Fe和H2SO4溶液 ⑧Na和O2
(1)由于浓度不同而发生不同氧化还原反应的是_____________________________________。
(2)由于温度不同而发生不同氧化还原反应的是______________________________。
(3)氧化还原反应不受浓度、温度影响的是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在P+CuSO4+H2O—→Cu3P+H3PO4+H2SO4(未配平)的反应中,7.5 mol CuSO4可氧化P的物质的量为________mol。生成1 mol Cu3P时,参加反应的P的物质的量为________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
某金属和硝酸反应,已知参加反应的被还原的硝酸和参加反应的硝酸的物质的量之比为1∶6,若已知还原产物唯一,则还原产物为( )
A.N2 B.N2O C.NO D.NO2
查看答案和解析>>
科目:高中化学 来源: 题型:
能在水溶液中大量共存的离子组是( )
A.H+、Fe3+、SO 、I-
、I-
B.H+、NH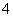 、HCO
、HCO 、NO
、NO
C.Ag+、K+、Cl-、SO
D.K+、AlO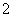 、Cl-、OH-
、Cl-、OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
水溶液中能大量共存的一组离子是( )
A.Na+、Al3+、Cl-、CO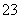
B.H+、Na+、Fe2+、MnO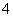
C.K+、Ca2+、Cl-、NO
D.K+、NH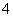 、OH-、SO
、OH-、SO
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式正确的是( )
A.NaAlO2溶液中滴加NaHCO3溶液:AlO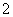 +HCO
+HCO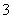 +H2O===Al(OH)3↓+CO
+H2O===Al(OH)3↓+CO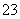
B.碘水中通入适量的SO2:I2+SO2+2H2O===2HI+SO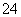 +2H+
+2H+
C.FeSO4溶液中滴加双氧水:2Fe2++2H2O2===2Fe3++O2↑+2H2O
D.Na2CO3发生水解反应:CO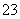 +2H2O===H2CO3+2OH-
+2H2O===H2CO3+2OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com