
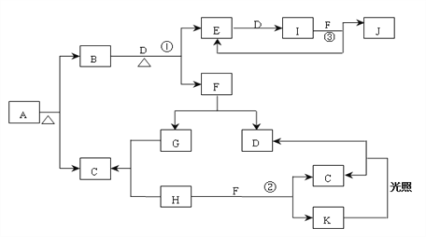
ЁОЬтФПЁПвбжЊЃКAЮЊе§бЮЃЌГЃЮТЁЂГЃбЙЯТЃЌBЁЂCЁЂDЁЂEЁЂGЁЂHЁЂIОљЮЊЦјЬхЃЌЦфжаDЁЂGЁЂHЮЊЕЅжЪЃЌЦјЬхBФмЪЙЪЊШѓКьЩЋЪЏШяЪджНБфРЖЃЌЦјЬхEБОЩэЮЊЮоЩЋЦјЬхЃЌЕЋЪЧгыПеЦјНгДЅЛсЩњГЩвЛжжКьзиЩЋЦјЬхIЃЌHЮЊЛЦТЬЩЋЦјЬхЁЃFдкГЃЮТЯТЪЧвЛжжЮоЩЋвКЬхЁЃCЁЂJЕФЫЎШмвКЗжБ№ЮЊСНжжЧПЫсЁЃЭМжаЗДгІЬѕМўЃЈГ§МгШШЭтЃЉОљвбТдШЅЁЃ
ЂХаДГіЫќУЧЕФЛЏбЇЪНЃК A________ЁЂC________ЁЂJ________ЃЛ
ЂЦЪЕбщЪвжЦБИЦјЬхBЕФЛЏбЇЗДгІЗНГЬЪНЮЊ______ЃЛ
ЂЧаДГіB+DЁњE+FЕФЛЏбЇЗДгІЗНГЬЪНЃК______ЃЛ
ЂШ JЕФХЈШмвКгыЕЅжЪAgЗДгІЕФРызгЗНГЬЪНЮЊЃК______ЃЛ
ЁОД№АИЁП NH4Cl HCl HNO3 2NH4Cl+Ca(OH)2![]() CaCl2+2NH3Ёќ+2H2O 4NH3+5O2
CaCl2+2NH3Ёќ+2H2O 4NH3+5O2![]() 4NO+6H2O Ag + 2H++NO3-
4NO+6H2O Ag + 2H++NO3-![]() Ag+ + NO2 Ёќ+H2O
Ag+ + NO2 Ёќ+H2O
ЁОНтЮіЁПAЮЊе§бЮЃЌГЃЮТЁЂГЃбЙЯТЃЌBЁЂCЁЂDЁЂEЁЂGЁЂHЁЂIОљЮЊЦјЬхЃЌЦфжаDЁЂGЁЂHЮЊЕЅжЪЃЌЦјЬхBФмЪЙЪЊШѓКьЩЋЪЏШяЪджНБфРЖЃЌBЮЊАБЦјЃЛЦјЬхEБОЩэЮЊЮоЩЋЦјЬхЃЌЕЋЪЧгыПеЦјНгДЅЛсЩњГЩвЛжжКьзиЩЋЦјЬхIЃЌEЮЊNOЃЌIЮЊNO2ЃЌИљОнПђЭМЃЌDЮЊбѕЦјЃЌJЕФЫЎШмвКЮЊЧПЫсЃЌJЮЊЯѕЫсЃЛHЮЊЛЦТЬЩЋЦјЬхЃЌHЮЊCl2ЁЃFдкГЃЮТЯТЪЧвЛжжЮоЩЋвКЬхЃЌFЮЊЫЎЃЌDЮЊбѕЦјЃЌдђGЮЊЧтЦјЃЌCЮЊТШЛЏЧтЃЌдђAЮЊТШЛЏяЇЃЌТШЦјгыЫЎЗДгІЩњГЩбЮЫсКЭДЮТШЫсЃЌдђKЮЊДЮТШЫсЁЃ
ЃЈ1ЃЉИљОнЩЯЪіЗжЮіЃЌAЮЊNH4Cl ЁЂCЮЊHClЁЂJЮЊHNO3ЃЌЙЪД№АИЮЊЃКNH4Cl ЃЛHClЃЛ HNO3ЃЛ
ЃЈ2ЃЉЪЕбщЪвжЦБИЦјЬхАБЦјЕФЛЏбЇЗДгІЗНГЬЪНЮЊ2NH4Cl+Ca(OH)2![]() CaCl2+2NH3Ёќ+2H2OЃЌЙЪД№АИЮЊЃК2NH4Cl+Ca(OH)2
CaCl2+2NH3Ёќ+2H2OЃЌЙЪД№АИЮЊЃК2NH4Cl+Ca(OH)2![]() CaCl2+2NH3Ёќ+2H2OЃЛ
CaCl2+2NH3Ёќ+2H2OЃЛ
ЃЈ3ЃЉB+DЁњE+FЕФЛЏбЇЗДгІЗНГЬЪНЮЊ4NH3+5O2![]() 4NO+6H2OЃЌЙЪД№АИЮЊЃК4NH3+5O2
4NO+6H2OЃЌЙЪД№АИЮЊЃК4NH3+5O2![]() 4NO+6H2OЃЛ
4NO+6H2OЃЛ
ЃЈ4ЃЉХЈЯѕЫсгыЕЅжЪAgЗДгІЕФРызгЗНГЬЪНЮЊAg + 2H++NO3-![]() Ag+ + NO2 Ёќ+H2OЃЌЙЪД№АИЮЊЃКAg + 2H++NO3-
Ag+ + NO2 Ёќ+H2OЃЌЙЪД№АИЮЊЃКAg + 2H++NO3-![]() Ag+ + NO2 Ёќ+H2OЁЃ
Ag+ + NO2 Ёќ+H2OЁЃ


 НђЧХНЬг§МЦЫуаЁзДдЊЯЕСаД№АИ
НђЧХНЬг§МЦЫуаЁзДдЊЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПбЮЫсгыаПЗДгІЪБЃЌШєМгШыЩйСППЩШмадЕФбЮЃЈCH3COOЃЉ2CuЃЌЖдИУЗДгІЕФЗДгІЫйТЪВњЩњЕФгАЯьЪЧЃЈ ЃЉ
A.діДѓ
B.МѕЩй
C.ВЛФмШЗЖЈ
D.ЮогАЯь
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЁАСНаЭЁБЩчЛсЃЌЬсГЋЁАЕЭЬМЁБЩњЛюЃЌЯТСагаЙиЬММАЬМЕФЛЏКЯЮяа№Ъіжае§ШЗЕФЪЧЃЈ ЃЉ
A.ЖўбѕЛЏЬМЪЧаЮГЩЫсгъЕФжївЊЦјЬх
B.Н№ИеЪЏЁЂЪЏФЋЖМЪЧЬМЕЅжЪЃЌСНепЬМдзгЕФХХСаЗНЪНЯрЭЌ
C.вЛбѕЛЏЬМКЌСПдіМгЛсЕМжТЮТЪваЇгІ
D.ДѓЦјжаЖўбѕЛЏЬМЕФЯћКФЭООЖжївЊЪЧТЬЩЋжВЮяЕФЙтКЯзїгУ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГГЇЗЯЫЎжаКЌ5.00ЁС10-3molЁЄL-1ЕФCr2O72-ЃЌЦфЖОадНЯДѓЁЃФГбаОПадбЇЯАаЁзщЮЊСЫБфЗЯЮЊБІЃЌНЋЗЯЫЎДІРэЕУЕНДХадВФСЯCr0.5Fe1.5FeO4ЃЈFeЕФЛЏКЯМлвРДЮЮЊ+3ЁЂ+2ЃЉЃЌЩшМЦСЫШчЯТЪЕбщСїГЬЃК
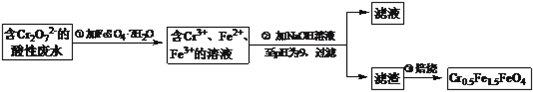
ЃЈ1ЃЉЕкЂйВНЗДгІЕФРызгЗНГЬЪНЪЧ____________________ЃЛ
ЃЈ2ЃЉЕкЂкВНжагУpHЪджНВтЖЈШмвКpHЕФВйзїЪЧЃК________________ЃЛ
ЃЈ3ЃЉЕкЂкВНЙ§ТЫЕУЕНЕФТЫдќжажївЊГЩЗжГ§Cr(OH)3ЭтЃЌЛЙга____________ЃЛ
ЃЈ4ЃЉгћЪЙ1LИУЗЯЫЎжаCr2O72-ЕФЭъШЋзЊЛЏЮЊCr0.5Fe1.5FeO4ЁЃРэТлЩЯашвЊМгШы____FeSO4ЁЄ7H2OЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЙигкNaHCO3ЕФЫЕЗЈе§ШЗЕФЪЧ
A. ЫзУћЪЧЫеДђЛђДПМю B. ЭЌЮТЖШЪБЕФШмНтЖШБШNa2CO3Дѓ
C. гыбЮЫсЗДгІЪББШNa2CO3Пь D. ШШЮШЖЈадЧПЃЌЪмШШФбвдЗжНт
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁП[ЮяжЪНсЙЙгыаджЪ]бѕдЊЫиКЭТБзхдЊЫиЖМФмаЮГЩЖржжЮяжЪЃЌЮвУЧПЩвдРћгУЫљбЇЮяжЪНсЙЙгыаджЪЕФЯрЙижЊЪЖШЅШЯЪЖКЭРэНтЁЃ
ЃЈ1ЃЉфхЕФМлЕчзгХХВМЪНЮЊ ЃЛPCl3ЕФПеМфЙЙаЭЮЊ ЁЃ
ЃЈ2ЃЉвбжЊCsICl2ВЛЮШЖЈЃЌЪмШШвзЗжНтЃЌЧуЯђгкЩњГЩОЇИёФмИќДѓЕФЮяжЪЃЌдђЫќАДЯТСа ЪНЗЂЩњ:
AЃЎCsICl2=CsCl+ICl BЃЎCsICl2=CsI+Cl2
ЃЈ3ЃЉИљОнЯТБэЕквЛЕчРыФмЪ§ОнХаЖЯЃКзюгаПЩФмЩњГЩНЯЮШЖЈЕФЕЅКЫбєРызгЕФТБЫидзгЪЧ__________
Зњ | ТШ | фх | Ет | |
ЕквЛЕчРыФмЃЈkJmolЉ1ЃЉ | 1681 | 1251 | 1140 | 1008 |
ЃЈ4ЃЉЯТСаЗжзгМШВЛДцдкsЉpІвМќЃЌвВВЛДцдкpЉpІаМќЕФЪЧ
AЃЎ HCl BЃЎHF CЃЎ SO2 DЃЎ SCl2
ЃЈ5ЃЉвбжЊCOCl2ЮЊЦНУцаЮЃЌдђCOCl2жааФЬМдзгЕФдгЛЏЙьЕРРраЭЮЊ ЃЌаДГіCOЕФЕШЕчзгЬхЕФЮЂСЃ ЃЈаДГі1ИіЃЉЁЃ
ЃЈ6ЃЉИЦдкбѕЦјжаШМЩеЪБЕУЕНвЛжжИЦЕФбѕЛЏЮяОЇЬхЃЌЦфНсЙЙШчЭМЫљЪОЃКгЩДЫПЩХаЖЯИУИЦЕФбѕЛЏЮяЕФЛЏбЇ ЪНЮЊ ЁЃвбжЊИУбѕЛЏЮяЕФУмЖШЪЧІбgcmЉ3ЃЌдђОЇАћРыЕУзюНќЕФСНИіИЦРызгМфЕФОрРыЮЊ cmЃЈжЛвЊЧѓСаЫуЪНЃЌВЛБиМЦЫуГіЪ§жЕЃЌАЂЗќМгЕТТоГЃЪ§ЮЊNAЃЉЁЃ

ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЛљДЁжЊЪЖЬюПеЃК
ЃЈ1ЃЉЫсгъЕФpHаЁгк______ЃЛЙшЫсФЦЕФЫЎШмвКЫзГЦ______ЃЛ
ЃЈ2ЃЉгавдЯТЮяжЪЃКЂйCu ЂкAl Ђл C ЂмЯЁСђЫс ЂнХЈСђЫс ЂоЯЁЯѕЫс ЂпХЈЯѕЫсЁЃ
МгШШЬѕМўЯТЃЌЂйКЭЂм______ЃЈЬюЁАФмЁБЛђепЁАВЛФмЁБЃЉЗДгІЃЛ
ГЃЮТЯТЃЌЂнКЭЂпПЩЪЂзАдк______ЃЈбЁЬюЂйЛђЂкЃЉШнЦїжаЃЛ
аДГіЂйгыЂоЗДгІЕФЛЏбЇЗНГЬЪН______ЃЛ
ЃЈ3ЃЉЪЕбщЪвгУMnO2гыХЈбЮЫсЗДгІжЦТШЦјЃЌдкИУЗДгІжаЃЌбѕЛЏМСЪЧ______ЃЌШчга1 mol Cl2ЩњГЩЃЌдђБЛбѕЛЏЕФHClЕФЮяжЪЕФСПЪЧ______molЃЌзЊвЦЕФЕчзгЪ§ФПЮЊ______ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПГЃЮТЯТЃЌ0.1 mol/LФГвЛдЊЫсЃЈHAЃЉШмвКжа![]() =1ЁС10-8ЃЌЯТСаа№Ъіе§ШЗЕФЪЧ
=1ЁС10-8ЃЌЯТСаа№Ъіе§ШЗЕФЪЧ
A. ШмвКжаЫЎЕчРыГіЕФc(H+)ЃН10-10 mol/L
B. ШмвКжаc(H+)ЃЋc(A-)ЃН0.1 mol/L
C. ШмвКжаМгШывЛЖЈСПCH3COONaОЇЬхЛђМгЫЎЯЁЪЭЃЌШмвКЕФc(OH-)ОљдіДѓ
D. гы0.05mol/LNaOHШмвКЕШЬхЛ§ЛьКЯКѓЫљЕУШмвКжаРызгХЈЖШДѓаЁЙиЯЕЮЊc(A-)ЃОc(Na+)ЃОc(OH-)ЃОc(H+)
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЧтдЊЫигыЦфЫћдЊЫиаЮГЩЕФЖўдЊЛЏКЯЮяГЦЮЊЧтЛЏЮяЃЌЯТУцЙигкЧтЛЏЮяЕФа№Ъіе§ШЗЕФЪЧЃЈ ЃЉ
AЃЎвЛИіD2OЗжзгЫљКЌЕФжазгЪ§ЮЊ8BЃЎNH3ЕФНсЙЙЪНЮЊHЁЊ![]() ЁЊH
ЁЊH
CЃЎHClЕФЕчзгЪНЮЊHЃЋ[![]() ]DЃЎШШЮШЖЈадЃКH2SЃОHI
]DЃЎШШЮШЖЈадЃКH2SЃОHI
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com