
| A. | Fe与A1的物质的量之比为1:1 | |
| B. | 混合气体中 NO为0.03mol,N2O0.12mol | |
| C. | 原HNO3溶液的浓度C=4.6mol/L | |
| D. | 反应中被还原的HNO3为0.18 mol |
分析 将Fe和Al的混合物溶于HNO3溶液中,得到NO、N2O混合气体,测得反应后溶液的pH为0,说明硝酸有剩余,故生成Al(NO3)3、Fe(NO3)3,再向所得溶液中加入过量NaOH溶液,铝离子完全转化为偏铝酸钠,得到沉淀5.35g为Fe(OH)3,其物质的量=$\frac{5.35g}{107g/mol}$=0.05mol,
A.根据原子守恒计算n(Fe),再根据m=nM计算m(Fe),进而计算m(Al),根据n=$\frac{m}{M}$计算n(Al),据此解答;
B.令混合气体中NO、N2O的物质的量分别为xmol、ymol,根据电子转移守恒及二者体积列方程解答;
C.根据N元素守恒n原(HNO3)=3n[Al(NO3)3]+3n[Fe(NO3)3]+n(NO)+2n(N2O)+n剩余(HNO3),进而计算浓度;
D.被还原的HNO3生成NO、N2O,根据氮元素守恒可知n被还原(HNO3)=n(NO)+2n(N2O).
解答 解:将Fe和Al的混合物溶于HNO3溶液中,得到NO、N2O混合气体,测得反应后溶液的pH为0,说明硝酸有剩余,故生成Al(NO3)3、Fe(NO3)3,再向所得溶液中加入过量NaOH溶液,铝离子完全转化为偏铝酸钠,得到沉淀5.35g为Fe(OH)3其物质的量=$\frac{5.35g}{107g/mol}$=0.05mol,
A.根据原子守恒n(Fe)=0.05mol,m(Fe)=0.05mol×56g/mol=2.8g,故m(Al)=6.85g-2.8g=4.05g,n(Al)=$\frac{4.05g}{27g/mol}$=0.15mol,故Fe与Al 的物质的量之比=0.05mol:0.15mol=1:3,故A错误;
B.令混合气体中NO、N2O的物质的量分别为xmol、ymol,根据电子转移守恒及二者体积,可得:
$\left\{\begin{array}{l}{x+y=\frac{3.36}{22.4}}\\{3x+8y=(0.05+0.15)×3}\end{array}\right.$,解得x=0.12、y=0.03,NO、N2O的物质的量分别为0.12mol,0.03mol,故B错误;
C.反应后溶液的pH为0,则n剩余(HNO3)=1mol/L×0.2L=0.2mol,根据N元素守恒n原(HNO3)=3n[Al(NO3)3]+3n[Fe(NO3)3]+n(NO)+2n(N2O)+n剩余(HNO3)=3×0.15mol+3×0.05mol+0.12mol+2×0.03mol+0.2mol=0.98mol,原HNO3溶液的浓度=$\frac{0.98mol}{0.2L}$=4.9mol/L,故C错误;
D.被还原的HNO3生成NO、N2O,根据氮元素守恒可知n被还原(HNO3)=n(NO)+2n(N2O)=0.12mol+2×0.03mol=0.18mol,故D正确,
故选D.
点评 本题考查混合物计算,判断反应过程是解题的关键,注意守恒思想的应用,侧重解题方法与思维能力考查,难度中等.


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:选择题
| A. | 纯净的苯酚是粉红色的晶体,65℃以上时能与水互溶 | |
| B. | 苯酚是生产电木的单体之一,与甲醛发生缩聚反应 | |
| C. | 苯酚比苯更易发生苯环上的取代反应 | |
| D. | 苯酚有毒,也能配制洗涤剂和软药膏 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
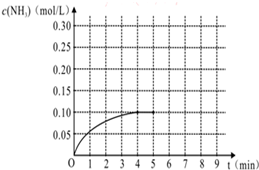 在一容积为4L的密闭容器中,加入0.4mol的N2和1.2mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g )△H<0,反应中NH3的物质的量浓度变化情况如图:
在一容积为4L的密闭容器中,加入0.4mol的N2和1.2mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g )△H<0,反应中NH3的物质的量浓度变化情况如图: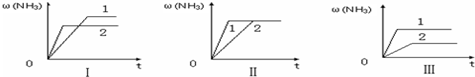
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过量的氢气与氧气 | B. | 过量的浓盐酸与二氧化锰 | ||
| C. | 过量的铜与浓硫酸 | D. | 过量的锌与18 mol/L硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钾、钠、镁等活泼金属着火时,不能用泡沫灭火器灭火 | |
| B. | 探究温度对硫代硫酸钠与硫酸反应速率的影响时,若先将两种溶液混合并计时,再用水浴加热至设定温度,则测得的反应速率偏低 | |
| C. | 滴定达终点时,发现滴定管尖嘴部分有悬滴,则测定结果偏小 | |
| D. | 为准确配制一定物质的量浓度的溶液,定容过程中向容量瓶内加蒸馏水至接近刻度线时,改用滴管滴加蒸馏水至刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:W<X<Y<Z | |
| B. | 简单氢化物的稳定性X>Y>Z | |
| C. | W、X、Y形成的化合物抑制水的电离 | |
| D. | m的分解产物中p为氧化产物,q为还原产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验序号 | I | II | III | IV | Ⅴ |
| 样品质量(g) | 3.06 | 6.12 | 9.18 | 12.24 | 15.30 |
| Ba(OH)2溶液体积(mL) | 300 | 300 | 300 | 300 | 300 |
| 生成沉淀的质量(g) | 5.91 | 11.82 | 17.73 | 23.64 | 23.64 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | N2O4和NO2的分子数比为1:2 | |
| B. | N2O4和NO2的浓度相等 | |
| C. | 体系的颜色不再改变 | |
| D. | 单位时间内有1molN2O4转化为NO2的同时,有2molNO2转化为N2O4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com