
 ʵ�����Ʊ��屽������ͼ��ʾװ�ã���գ�
ʵ�����Ʊ��屽������ͼ��ʾװ�ã���գ� ��
������ ʵ�����Ʊ��屽���ñ���Һ���������������������·���ȡ����Ӧ�����屽���廯�⣬����װ��ͼ��֪�������屽��ͬ�������廯������������ٲ�����ӷ���������Dװ����ʯ����죬E�е�������������廯��������β��������������Һ���գ��ر�C��Fʱ�������廯�⼫������ˮ�����ƿ�е�ˮ�ᵹ����������ƿ��
��1�������屽�����ʿ�֪���屽��һ���ܶȱ�ˮ�����ɫҺ�壬��ʵ������Ϊ�ܽ��˲���������Ժ�ɫ����������ƿ�������������廯�������������廯��������������������ȡ����Ӧ�����屽���廯�⣻
��2����Ӧ�������廯����������ʯ����Һ����ʯ����Һ���ɫ���廯������ͨ����������Һ���ܲ���dz��ɫ������
��3������������Һ�������廯�⣬���õ�©���ܷ�ֹ����������
��4��������ƿ�е��屽��������������廯�⣬������NaOH��Һ��ȥ���屽������ˮ���ܶȱ�ˮ�ݴ˴��⣮
��� �⣺ʵ�����Ʊ��屽���ñ���Һ���������������������·���ȡ����Ӧ�����屽���廯�⣬����װ��ͼ��֪�������屽��ͬ�������廯������������ٲ�����ӷ���������Dװ����ʯ����죬E�е�������������廯��������β��������������Һ���գ��ر�C��Fʱ�������廯�⼫������ˮ�����ƿ�е�ˮ�ᵹ����������ƿ��
��1����������ƿ�������������廯�������������廯��������������������ȡ����Ӧ�����屽���廯�⣬�����йط�Ӧ�Ļ�ѧ����ʽ�ֱ���2Fe+3Br2=2FeBr3��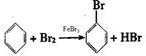 ��
��
�ʴ�Ϊ��2Fe+3Br2=2FeBr3�� ��
��
��2���������ɵ��廯�⼫�ӷ�������ˮ�����ԣ�����ɫʯ����Һ��죬�廯������ˮ����������Ӧ�����廯������ɫ���ģ���ʵ����������Һ���е���ɫ�������ɣ�����D��ʯ����Һ��죬E�ܳ���dz��ɫ������
�ʴ�Ϊ��D��ʯ����Һ��죬E�ܳ���dz��ɫ������
��3������������Һ�������廯�⣬���õ�©���ܷ�ֹ��������������F�������������ų����廯�����壬��ֹ��Ⱦ������ͬʱ�ܷ�ֹ������
�ʴ�Ϊ�������ų����廯�����壬��ֹ��Ⱦ������ͬʱ�ܷ�ֹ������
��4���屽�����������������NaOH��Һ��ȥ���屽������ˮ���ܶȱ�ˮ���ӹ�����������Һ�Ļ����Һ�����Һ©���У����ú��屽�ӷ�Һ©�����¿ڷų����ɣ��ʴ�Ϊ��NaOH��Һ��
���� �����Ǹ߿��еij������ͣ������е��Ѷȵ����⣬�����ۺ���ǿ���������У���ע�ض�ѧ��������֪ʶ�����ѵ����ͬʱ�����ض�ѧ�������������ͽ��ⷽ����ָ����ѵ��������������ѧ�����Ͻ��淶��ʵ�����������Ҳ���������ѧ����ѧ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ȻCu�ܵ��磬��Cu�Ƿǵ���� | |
| B�� | AgCl��Ȼ������ˮ����AgCl�ǵ���� | |
| C�� | SO3��NH3��ˮ��Һ���ܵ��磬����SO3��NH3���ǵ���� | |
| D�� | KNO3��Һ�ܵ��磬�����������Һ�ǵ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����0.025 mol P2O5 | |
| B�� | ���� P2O3���ͷŵ�����Ϊ��Y-0.05X�� kJ | |
| C�� | 2P��s��+$\frac{3}{2}$O2��g��=P2O3��s����H=-��40Y-2X��kJ•mol-1 | |
| D�� | ���ɵ� P2O3�� P2O5������֮��Ϊ 1��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
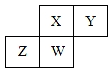 ������Ԫ��X��Y��Z��W��Ԫ�����ڱ��е����λ����ͼ��ʾ������Wԭ�ӵ���������������������������������˵������ȷ���ǣ�������
������Ԫ��X��Y��Z��W��Ԫ�����ڱ��е����λ����ͼ��ʾ������Wԭ�ӵ���������������������������������˵������ȷ���ǣ�������| A�� | ԭ�Ӱ뾶��Z��W��X��Y | |
| B�� | ����������Ӧˮ��������ԣ�X��W��Z | |
| C�� | �����̬�⻯������ȶ��ԣ�Y��X��W��Z | |
| D�� | ZY2�����ۻ���Һ̬Y3��������˷����Ӽ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 5�� | B�� | 4�� | C�� | 3�� | D�� | 2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ����ѧ�� | ��N-H | ��N-N | ��N��N | ��O-H |
| �����ܣ�kJ��mol-1�� | ��390 | ��190 | ��946 | ��460 |

| ʱ��/min | ��0 | ��5 | ��10 | ��15 | ��20 | ��25 | ��30 |
| ��c��X��/��mol/L�� | ��0.2 | ��c | ��0.6 | ��0.6 | ��1.0 | ��c1 | ��c1 |
| ��c��Y��/��mol/L�� | ��0.6 | ��c | ��0.4 | ��0.4 | ��0.4 | ��c2 | ��c2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com