
某气态烷烃和气态炔烃的混合烃2 L,完全燃烧后生成CO2 2.8 L、水蒸气3.2 L(同压且同在200℃下测定),该混合烃为( )
A.CH4、C2H2 B.C2H6、C2H2
C.C3H8、C3H4 D.CH4、C3H4
科目:高中化学 来源: 题型:
以乙炔为原料,通过下图所示步骤能合成有机中间体E(转化过程中的反应条件及部分产物已略去):
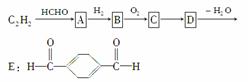
其中,A,B,C,D分别代表一种有机物,B的化学式为C4H10O2,分子中无甲基。
请回答下列问题:
(1)A生成B的化学反应类型是____________。
(2)写出生成A的化学反应方程式
________________________________________________________________________
________________________________________________________________________。
(3)B在浓硫酸催化下加热,可生成多种有机产物。写出2种相对分子质量比A小的有机产物的结构简式:__________________、__________________、
__________________。
(4)写出C生成D的化学反应方程式:
________________________________________________________________________
________________________________________________________________________。
(5)含有苯环,且与E互为同分异构体的酯有____________种,写出其中一种同分异构体的结构简
式:________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
若要使0.5 mol甲烷完全和氯气发生取代反应,并生成相同物质的量的四种取代物,则需要氯气的物质的量为( )
A.2.5 mol B.2 mol C.1.25 mol D.0.5 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
环丙烷可作为全身麻醉剂,环己烷是重要的有机溶剂。下面是部分环烷烃及烷烃衍生物的结构简式、键线式和某些有机化合物的反应式(其中Pt、Ni是催化剂):
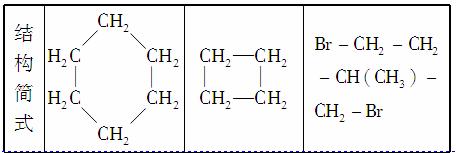
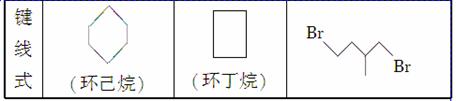

回答下列问题:
(1)环烷烃与__________________是同分异构体。
(2)从反应①~③可以看出,最容易发生开环加成反应的环烷烃是______________(填名称),判断依据为_________________________________。
(3)环烷烃还可与卤素单质、卤化氢发生类似的开环加成反应,如环丁烷与HBr在一定条件下反应,其化学方程式为______________________________
________________________________________________________________________(不需注明反应条件)。
(4)写出鉴别环丙烷与丙烯的一种方法,试剂______;现象与结论_______________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某探究小组利用丙酮的溴代反应(CH3COCH3+Br2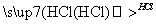 CH3COCH2Br+HBr)来研究反应物浓度与反应速率的关系。反应速率v(Br2)通过测定溴的颜色消失所需的时间来确定。在一定温度下,获得如下实验数据:
CH3COCH2Br+HBr)来研究反应物浓度与反应速率的关系。反应速率v(Br2)通过测定溴的颜色消失所需的时间来确定。在一定温度下,获得如下实验数据:
| 实验 序号 | 初始浓度c/mol·L-1 | 溴颜色消失 所需时间t/s | ||
| CH3COCH3 | HCl | Br2 | ||
| ① | 0.80 | 0.20 | 0.001 0 | 290 |
| ② | 1.60 | 0.20 | 0.001 0 | 145 |
| ③ | 0.80 | 0.40 | 0.001 0 | 145 |
| ④ | 0.80 | 0.20 | 0.002 0 | 580 |
分析实验数据所得出的结论不正确的是( )
A.增大[CH3COCH3],v(Br2)增大
B.实验②和③的v(Br2)相等
C.增大[HCl],v(Br2)增大
D.增大[Br2],v(Br2)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
根据碰撞理论,分子在发生反应时必须要进行有效碰撞。那些具有足够高能量,能发生有效碰撞的分子称为活化分子,要使普通分子成为活化分子所需最小能量称为活化能(Ea)。一定温度下气体分子中的活化分子百分数是一定的,而催化剂可以改变活化能的大小。如图表示298.15 K时,N2、H2与NH3的平均能量与合成氨反应的活化能的曲线图,据图回答:

(1)若反应中生成2 mol氨,则反应________(填“吸热”或“放热”)________kJ。
(2)在图中曲线________(填“a”或“b”)表示加入铁触媒的能量变化曲线,铁触媒能加快反应速率的原理是_____________________________________________________________
________________________________________________________________________。
(3)目前合成氨工业广泛采用的反应条件500℃、20 MPa~50 MPa、铁触媒,反应转化率不超过50%,工业上为了进一步提高氨气产率,你认为下列措施最经济可行的是
________________________________________________________________________。
A.降低反应温度,让反应向着有利于氨气生成的方向进行
B.升高温度,让更多的分子变成活化分子
C.寻求能在更低的温度下有很强催化活性的新型催化剂
D.寻求新型耐高压材料,将压强增大一倍
查看答案和解析>>
科目:高中化学 来源: 题型:
氢氧燃料电池已用于航天飞机。以20%NaOH溶液为电解质溶液的这种电池在使用时的电极反应如下:
2H2+4OH--4 e-=4H2O O2+2H2O+4
e-=4H2O O2+2H2O+4 e-=4OH- 据此判断,下列说法中正确的是
e-=4OH- 据此判断,下列说法中正确的是
A.H2在正极发生氧化反应 B.燃料电池属二次电池
C.燃料电池的能量转化率常达100% D.供电时产生无污染的水,属于环境友好电池
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com