
| A. | ②①③④ | B. | ④③②① | C. | ④②①③ | D. | ③②④① |
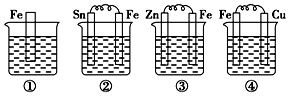
分析 ①铁为活泼金属,可发生的是化学腐蚀,
②铁做负极,锡做正极,电解质溶液为海水,则负极铁发生氧化反应,正极发生还原反应,
③锌比铁活泼,做原电池的负极而被氧化,铁做正极被保护,
④铁做负极被腐蚀,铜做正极,
电化学腐蚀的速率大于化学腐蚀的速率,金属做原电池正极时得到保护.
解答 解:根据图知:①铁为活泼金属,可发生的是化学腐蚀,
②B为原电池装置,Fe较活泼为原电池的负极,发生氧化反应被腐蚀,
③Zn比Fe活泼,形成原电池反应,锌被氧化,铁做正极被保护,
④铁做负极发生氧化反应被腐蚀,铜做正极;
①发生化学腐蚀,②发生电化学腐蚀,③锌比铁活泼,铁做原电池的正极而被保护,④发生电化学腐蚀,其中两个电极活泼些相差越大铁腐蚀速率越大,②④都是铁做负极被腐蚀,④中电极金属活泼性相差大所以腐蚀速率快,
电化学腐蚀的速率大于化学腐蚀的速率,腐蚀速率由快到慢的顺序为④>②>①>③,
故选:C.
点评 本题考查金属的电化学腐蚀与防护,题目难度不大,注意金属的电化学腐蚀与化学腐蚀的区别,以及比较金属腐蚀快慢的方法.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 燃烧时只发生了物理变化 | |
| B. | 氧化时,氯元素从化合态转变为游离态 | |
| C. | 用CCl4萃取碘的过程中,没有化学变化发生 | |
| D. | 可以用四氯化碳或酒精作为萃取剂将碘单质从碘水中萃取出来 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性溶液中:Cl-、SO42-、Fe3+、Mg2+ | |
| B. | 使酚酞变红的溶液中:Na+、CO32-、Cl-、Al3+ | |
| C. | 1.0 mol•L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- | |
| D. | 1.0 mol•L-1的CuSO4溶液:H+、Ba2+、AlO2-、NH3•H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
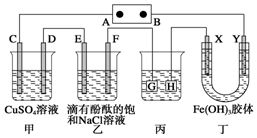 如图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.
如图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应中 KMnO4被氧化 | |
| B. | 氧化产物与还原产物的物质的量之比为 2:5 | |
| C. | 每生成 1 mol Cl2时,反应中转移的电子为 2 mol | |
| D. | 每消耗 16 molHCl 时,其中作氧化剂的 HCl 是 10 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入过量SO2:H+、Cl-、ClO-、HSO3- | |
| B. | 通入过量FeSO4溶液:Fe2+、H+SO42-、ClO- | |
| C. | 加入少量Al2(SO4)3溶液:Al3+、H+、ClO-、SO42- | |
| D. | 加入少量Na2O2固体:Na+、Cl-、ClO-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
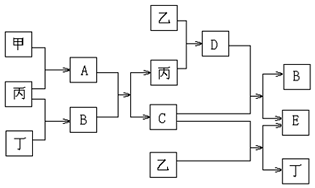
| 实验序号 | 甲 | 乙 | 丙 |
| 混合物质量/mg | 255 | 385 | 459 |
| 气体体积/mL | 280 | 336 | 336 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com