
 ��
������ A��B��C��D��EΪԭ��������������Ķ�����Ԫ�أ���֪A��B��E��ԭ������㹲��11�����ӣ���������Ԫ�ص�����������Ӧ��ˮ����֮���������ܷ�Ӧ�����κ�ˮ����AΪNa��BΪAl��E������������Ϊ11-1-3=7����EΪClԪ�أ�CԪ�ص������������ȴ�����������4����CΪSiԪ�أ�DԪ��ԭ�Ӵ�����������������������3������������Ϊ5����֪DΪP���Դ������
��� �⣺��1��������������֪��AΪNa��BΪAl��CΪSi��DΪP��EΪCl��
�ʴ�Ϊ��Na��Si��Cl��
��2��EԪ��+1�ۺ�����ΪHClO�������ʽΪ ��
��
�ʴ�Ϊ�� ��
��
��3��A��B��Ԫ������������Ӧ��ˮ�������Ӧ�����ӷ���ʽΪAl��OH��3+OH-�TAlO2-+2H2O��
�ʴ�Ϊ��Al��OH��3+OH-�TAlO2-+2H2O��
���� ���⿼��λ�á��ṹ�����ʣ�Ϊ��Ƶ���㣬����Ԫ�ػ�����֪ʶ��Ԫ�ص����ʡ�ԭ�ӽṹ�ƶ�Ԫ��Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע��Ԫ�ػ�����֪ʶ��Ӧ�ã���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaCl | B�� | MgCl2 | C�� | AlC13 | D�� | FcC12 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A | B | C | D |
 |  |  |  |
| �����շ��ɼ���ë���������α | ��īд�ֻ����ɳ��ò���ɫ | ֽ����ֽԭ�ϵ���Ҫ�ɷ־�����ά�� | ��ʯ��������̨�Ĺ����ǻ�ѧ�仯 |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
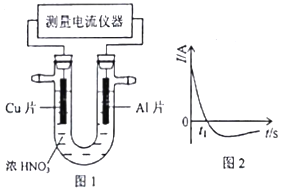 C��N��O��Na��Al��Si��S��Cl�dz����İ���Ԫ��
C��N��O��Na��Al��Si��S��Cl�dz����İ���Ԫ�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
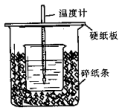 ��50mL0.50mol/L������50mL0.55mol/LNaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȣ��ش��������⣺
��50mL0.50mol/L������50mL0.55mol/LNaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȣ��ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ӱ���ģ�ͣ� | |
| B�� | ԭ�Ӻ�����18�����ӵ�ԭ�ӣ�${\;}_{17}^{35}$Cl | |
| C�� | 1��2-��������Ľṹ��ʽ��C2H4Br2 | |
| D�� | �����������ʽ��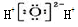 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��֪ 0.2 mol•L-1��NaHSO3��Һ��pH��7������Һ��һ���У�c��H2SO3����c��SO32-�� | |
| B�� | 0.02 mol/L��NaOH��Һ��0.02 mol/L��NaHC2O4��Һ��������Һ��2c��OH-��+c��C2O42-��=c��HC2O4-��+2c��H+�� | |
| C�� | ��ˮ����ε�����������Һ��pH=7������Һ��c��NH4+��=c��Cl-�� | |
| D�� | �����ᣨHN3����������������0.1 mol•L-1NaN3ˮ��Һ������Ũ�ȴ�С˳��Ϊ��c��Na+����c��N3-����c��OH-����c��H+�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com