
【题目】五种短周期元素A、B、C、D、E的原子序数依次增大,A和C同族,B和D 同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物在水中呈中性。回答下列问题:
(1)五种元素中,原子半径最大的是 ,非金属性最强的是 (填元素符号);
(2)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是 (用化学式表示);
(3)A和E形成的化合物与A和B形成的化合物反应,产物的化学式为 ,其中存在的化学键类型为 ;
(4)D最高价氧化物的水化物的化学式为 ;
(5)单质D在充足的单质E中燃烧,反应的化学方程式为 ;D在不充足的E中燃烧,生成的主要产物的化学式为 ;
(6)单质E与水反应的离子方程式为 。
【答案】(1)Na(2分) Cl (2分) (2)PH3(2分)
(3)NH4Cl(2分) 离子键和共价键(2分)
(4)H3PO4(2分) (5)2P+5Cl2![]() 2PCl5(2分) PCl3(2分)
2PCl5(2分) PCl3(2分)
(6)Cl2+H2O=H++Cl-+HClO(2分)
【解析】
试题根据题目所给的信息,A和BDE均可以形成共价型化合物,可知A是H元素,B是N元素(AB形成化合物的水溶液显碱性),C是Na元素,D是P元素,E是Cl元素。
(1)根据原子半径变化规律,可知Na的原子半径最大;Cl的非金属性最强;
(2)H与N、P、Cl形成的氢化物NH3、PH3、HCl,PH3最不稳定(P的非金属新最弱);
(3)AE形成的化合物是HCl,A和B形成的化合物是NH3,二者反应的到的盐是NH4Cl,存在的化学键:离子键和共价键;
(4)P的最高价是+5价,最高价氧化物水化物的化学式为H3PO4。


科目:高中化学 来源: 题型:
【题目】化学与生活密切相关。下列说法错误的是
A.用甲醛浸泡水产品以免腐烂
B.棉花、麻、蚕丝、羊毛都是天然纤维
C.聚乙烯塑料袋可用于包装产品
D.石油裂化的主要目的是提高汽油的产量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在冶金工业上,均不能用通常化学还原剂制得的金属组是
A. K、Na、Mg、Al.B. K、Na、Zn、Fe
C. Zn、Fe、Cu、AgD. Mg、Al、Zn、Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.施安卡因(G)是一种抗心律失常药物,可由下列路线合成.
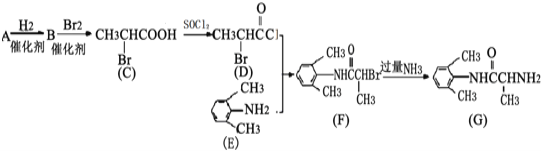
(1)已知A可以通过加聚反应生成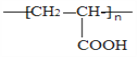 ,则A中所含官能团的名称是__________.
,则A中所含官能团的名称是__________.
(2)B的结构简式为___________;用系统命名法给C命名为___________.
(3)C与足量NaOH醇溶液共热时反应的化学方程式为____________________________.F→G的反应类型为___________.
Ⅱ.H是C的同系物,其核磁共振氢谱有两个峰.按如下路线,由H可合成高聚物V
![]()
(4)H的结构简式为___________.
(5)Q→V反应的化学方程式___________________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在水溶液中1 mol Cl-、ClOx-(x=1,2,3,4)的能量(kJ)相对大小如图所示。下列有关说法正确的是
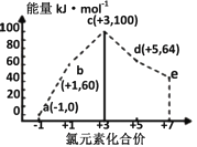
A. a、b、c、d、e中,c最稳定
B. b→a+c反应的活化能为反应物能量减生成物能量
C. b→a+d反应的热化学方程式为:3ClO-(aq)=ClO3-(aq)+2Cl-(aq)ΔH=+116 kJ·mol-1
D. 一定温度下,Cl2与NaOH溶液反应生成的产物有a、b、d,溶液中a、b、d的浓度之比可能为11∶1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇分子结构中,各化学键如图所示。关于乙醇在各种反应中断键的说法不正确的是( )
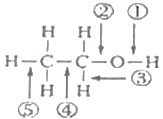
A. 和浓硫酸共热至170℃时,②、⑤键断裂 B. 和金属钠反应时,①键断裂
C. 在银催化条件下与O2反应时,①、③键断裂 D. 乙醇燃烧时,②、④键渐裂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质或离子检验的叙述正确的是
A. 气体通过无水硫酸铜粉末,粉末变蓝,证明原气体中含有水蒸气
B. 在溶液中加KSCN溶液,溶液显红色,证明原溶液中有Fe3+,无Fe2+
C. 灼烧白色粉末,火焰呈黄色,证明原粉末中有Na+,无K+
D. 向某无色溶液中加入盐酸,产生无色无味气体,将气体通入澄清石灰水,溶液变浑浊,证明原溶液一定含有![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。下图是元素周期表的一部分,回答下列问题:
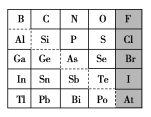
(1)元素Ga在元素周期表中的位置为:第________周期第________族。
(2)Sn的最高正价为________,Cl的最高价氧化物对应水化物的化学式为________,Bi的最高价氧化物为________。
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是________元素(填元素符号)。
②H3AsO4、H2SeO4的酸性强弱:H3AsO4________(填“>”“<”或“=”)H2SeO4。
③氢化物的还原性:H2O________(填“>”“<”或“=”)H2S。
④原子半径比较:N________(填“>”“<”或“=”)Si。
(4)从下列试剂中选择最佳试剂组合,比较C、Si的非金属性强弱___________________ (可供选择的药品有:CaCO3固体、稀硫酸、盐酸、饱和NaHCO3溶液、饱和Na2CO3溶液、硅酸钠溶液)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com