

 2NH3.
2NH3.分析 (1)合成塔中氮气和氢气反应生成氨气,该反应为可逆反应;
(2)根据题干中的生产流程图知,原料气氮气和氢气,经过氨的合成、氨的分离,循环利用的为氮气和氢气的混合气;
(3)氧化炉中氨的催化氧化,产物是一氧化氮和水,据此来书写反应方程式;
(4)NO2和NH3反应:8NH3+6NO2$\frac{\underline{\;催化剂\;}}{\;}$7N2+12H2O中,NH3中N元素的化合价由-3升高为0价,NO2中N元素的化合价由+5价降低为0价,转移电子数为24e-,以此来解答.
(5)吸收塔中通入空气的作用是使NO2和NO全部转化为HNO3,根据4NO+3O2+2H2O=4HNO3;4NO2+O2+2H2O=4HNO3、以及空气中氧气的体积体积分数为21%进行计算.
解答 解:(1)合成塔中氮气和氢气反应:3H2+N2 2NH3,故答案为:3H2+N2
2NH3,故答案为:3H2+N2 2NH3;
2NH3;
(2)合成氨反应是一个可逆反应,氨气极易挥发,氨分离器中压强约为15MPa,温度约为-20℃,分离氨应用了氨的易挥发性质,根据题干中的生产流程图知,经过氨的合成、氨的分离,分离出的是氨气,循环利用的为氮气和氢气的混合气,
故答案为:易挥发;N2、H2;
(3)氧化炉中发生的反应是氨的催化氧化反应,原理方程式为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,故答案为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
(4)NO2和NH3反应NH3中N元素的化合价由-3升高为0价,NO2中N元素的化合价由+4价降低为0价,生成氮气和水,反应方程式为:8NH3+6NO2$\frac{\underline{\;催化剂\;}}{\;}$7N2+12H2O,6molNO2参加反应转移电子数为24mole-,当有5.6LNO2被还原时,被还原的氮气的物质的量为:$\frac{5.6L}{22.4L/mol}$=0.25mol,转移电子的物质的量为0.25mol×24×$\frac{1}{6}$=1mol,
故答案为:1;
(5)氧化炉中出来的气体,先降温再进入吸收塔,吸收塔中通入空气发生反应2NO+O2=2NO2;4NO+3O2+2H2O=4HNO3;4NO2+O2+2H2O=4HNO3,所以通入空气作用为使NO2和NO全部转化为HNO3,进入吸收塔的气体的体积分数为NO210.0%,NO 1.32%,其余为N2、水蒸气等,当进入氧化炉中气体为10m3时,NO2体积为10m3×10%=0.1m3,需氧气:0.1m3×$\frac{1}{4}$,NO体积为10m3×1.32%=0.0132m3,需氧气:0.0132m3×$\frac{3}{4}$,空气中氧气的体积体积分数为21%,最少需要空气的体积为$\frac{0.1{m}^{3}×\frac{1}{4}+0.0132{m}^{3}×\frac{3}{4}}{21%}$≈1.66m3,
故答案为:使NO2和NO全部转化为HNO3;1.66.
点评 本题主要考查了合成氨工业,题目综合性较强,题目难度中等,掌握合成氨工业的流程,掌握氮及其化合物的性质是解答本题的关键,综合考查了学生具有分析和解决问题的能力.


科目:高中化学 来源: 题型:选择题
| A. | Q1=Q2=Q3 | B. | Q2>Q1>Q3 | C. | Q2>Q3>Q1 | D. | Q2=Q3>Q1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
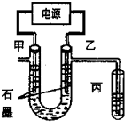 CuCl2溶液中的铜主要以Cu (H2O)42+、CuCl42-形式存在,它们间有如下转化关系:Cu (H2O)42+ (蓝色)+4Cl-?CuCl42- (黄色)+4H2O;电解不同浓度的CuCl2溶液,均可看做Cu2+、Cl-直接放电.下图为电解浓度较大CuCl2溶液的装置,实验开始后,观察到丙中的KI-淀粉溶液慢慢变蓝.回答下列问题:
CuCl2溶液中的铜主要以Cu (H2O)42+、CuCl42-形式存在,它们间有如下转化关系:Cu (H2O)42+ (蓝色)+4Cl-?CuCl42- (黄色)+4H2O;电解不同浓度的CuCl2溶液,均可看做Cu2+、Cl-直接放电.下图为电解浓度较大CuCl2溶液的装置,实验开始后,观察到丙中的KI-淀粉溶液慢慢变蓝.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 向0.1mol-1•LNa2CO3溶液中通入适量CO2气体后:c(Na+)=2[c(HCO3-)+c(CO32-)+c(H${\;}_{{2}_{\;}}$CO3)] | |
| B. | 在pH=8的NaB溶液中:c(Na+)-c(B-)=9.9×10-7mol•L-1 | |
| C. | 在0.1mol•L-1NaHSO3溶液中通入少量NH3气体后:c(Na+)+c(H+)=c(HSO-3)+2c(SO32-) | |
| D. | 在0.1mol•L-1的氯化铵溶液中:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
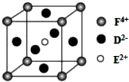 A、B、C、D、E、F是前四周期原子序数依次增大的六种元素.A元素原子的核外电子数等于其电子层数,B元素基态原子有三个能级且各能级电子数相同,A与D可形成两种常见液态化合物G、H,其原子数之比分别为1:1和2:1,E元素原子的K、L层电子数之和等于其M、N层电子数之和,F被称为继铁、铝之后的第三金属,可用于制造飞机、火箭、人造卫星、宇宙飞船等领域.请回答下列各题(涉及元素请用相应化学符号表示):
A、B、C、D、E、F是前四周期原子序数依次增大的六种元素.A元素原子的核外电子数等于其电子层数,B元素基态原子有三个能级且各能级电子数相同,A与D可形成两种常见液态化合物G、H,其原子数之比分别为1:1和2:1,E元素原子的K、L层电子数之和等于其M、N层电子数之和,F被称为继铁、铝之后的第三金属,可用于制造飞机、火箭、人造卫星、宇宙飞船等领域.请回答下列各题(涉及元素请用相应化学符号表示):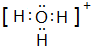 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | p(Ne)>p(N2)>p(O2) | B. | p(O2)>p(Ne)>p(N2) | C. | p(N2)>p(O2)>p(Ne) | D. | p(N2)>p(Ne)>p(O2) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤⑦ | B. | ①②③⑥ | C. | ②③④⑤ | D. | ①④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业用焦炭在高温下还原二氧化硅制得高纯硅 | |
| B. | SiO2可用于制造光导纤维 | |
| C. | 钠是一种强还原剂,可以把钛、锆、铌等从其熔融盐中置换出来 | |
| D. | 氧化镁熔点高达250℃,是优质的耐高温材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com