
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
 某化学兴趣小组,通过右图装置进行硫酸与铜反应的实验探究.
某化学兴趣小组,通过右图装置进行硫酸与铜反应的实验探究.| 实验编号 | 实验操作 | 实验现象 |
| 1 | 将Cu丝与稀H2SO4接触,加热 | 试管B中溶液无明显变化 |
| 2 | 将Cu丝与浓H2SO4接触,加热 | 试管B中溶液褪色 |
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:022
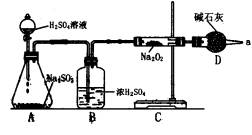
(1)怎样确定反应中是否有O2生成?
(2)装置B的作用是________,装置D的作用是________。
(3)该同学为了确定另一产物是Na2SO3还是Na2SO4,设计实验如下:
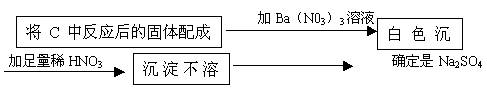
确定是Na2SO4 你认为该同学的实验是否合理________,理由是________。
若你认为不合理,请你设计一个合理实验来确定产物(括号内填加人物质,方框内填现象):若你认为合理,可不回答此问。
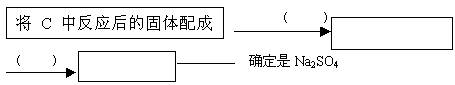
查看答案和解析>>
科目:高中化学 来源: 题型:
NaCl+H2SO4(浓)![]() NaHSO4+HCl↑
NaHSO4+HCl↑
2NaCl+H2SO4![]() Na2SO4+2HCl↑
Na2SO4+2HCl↑
现将117 g食盐与含98 g H2SO4的浓硫酸一并反应,计算可制取的HCl的体积(标准状况下)。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)怎样确定反应中是否有O2生成?
(2)装置B的作用是__________________,装置D的作用是__________________。

(3)该同学为了确定另一产物是Na2SO3还是Na2SO4,设计实验如下:
![]()
![]()
你认为该同学的实验是否合理__________,理由是______________________________。
若你认为不合理,请你设计一个合理实验来确定产物(括号内填加入物质,方框内填现象);若你认为合理,可不回答此问。
![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com