
| A. | 当生成的沉淀量达到最大时,消耗NaOH溶液的体积V≥100 mL | |
| B. | 当金属全部溶解时,参加反应的硝酸的物质的量一定是0.4mol | |
| C. | 参加反应的金属的总质量为9.6 g>m>3.6 g | |
| D. | 当金属全部溶解时收集到NO气体的体积一定为2.24 L |
分析 将一定量的镁和铜组成的混合物加入到稀HNO3中,金属完全溶解(假设反应中还原产物只有NO),发生反应:3Mg+8HNO3 (稀)=3Mg(NO3)2+2NO↑+4H2O、3Cu+8HNO3 (稀)=3Cu(NO3)2+2NO↑+4H2O;
向反应后的溶液中加入过量的3mol/L NaOH溶液至沉淀完全,发生反应:Mg(NO3)2+2NaOH=Mg(OH)2↓+2NaNO3、Cu(NO3)2+2NaOH=Cu(OH)2↓+2NaNO3,沉淀为氢氧化镁和氢氧化铜,生成沉淀的质量比原合金的质量增加5.1g,则氢氧化镁和氢氧化铜含有氢氧根的质量为5.1g,氢氧根的物质的量为:$\frac{5.1g}{17g/mol}$=0.3mol,根据电子转移守恒,则镁和铜的总的物质的量为0.15mol,
A.加入的氢氧化钠可能中和未反应的硝酸;
B.根据方程式可知参加反应的n反应(HNO3)=$\frac{8}{3}$n(金属);
C.利用极限法假定全为镁、全为铜计算判断;
D.根据电子转移守恒计算NO物质的量,结合气体不一定是标准状况判断.
解答 解:将一定量的镁和铜组成的混合物加入到稀HNO3中,金属完全溶解(假设反应中还原产物只有NO),发生反应:3Mg+8HNO3 (稀)=3Mg(NO3)2+2NO↑+4H2O、3Cu+8HNO3 (稀)=3Cu(NO3)2+2NO↑+4H2O;
向反应后的溶液中加入过量的3mol/L NaOH溶液至沉淀完全,发生反应:Mg(NO3)2+2NaOH=Mg(OH)2↓+2NaNO3;Cu(NO3)2+2NaOH=Cu(OH)2↓+2NaNO3,沉淀为氢氧化镁和氢氧化铜,生成沉淀的质量比原合金的质量增加5.1g,则氢氧化镁和氢氧化铜含有氢氧根的质量为5.1g,氢氧根的物质的量为:$\frac{5.1g}{17g/mol}$=0.3mol,根据电子转移守恒,则镁和铜的总的物质的量为0.15mol,
A.若硝酸无剩余,则参加反应氢氧化钠的物质的量等于0.3mol,需要氢氧化钠溶液体积=$\frac{0.3mol}{3mol/L}$=0.1L=100mL,硝酸若有剩余,消耗的氢氧化钠溶液体积大于100mL,故A正确;
B.根据方程式可知参加反应的n反应(HNO3)=$\frac{8}{3}$n(金属)=0.15mol×$\frac{8}{3}$=0.4mol,故B正确;
C.镁和铜的总的物质的量为0.15mol,假定全为镁,质量为0.15mol×24g/mol=3.6g,若全为铜,质量为0.15mol×64g/mol=9.6g,所以参加反应的金属的总质量(m)为3.6g<m<9.6g,故C正确;
D.镁和铜的总的物质的量为0.15mol,根据电子转移守恒可知生成的NO物质的量为:$\frac{0.15mol×2}{3}$=0.1mol,若为标准状况下,生成NO的体积为0.1mol×22.4L/mol=2.24L,但NO不一定处于标准状况,收集到NO气体的体积不一定为2.24L,故D错误;
故选D.
点评 本题主要考查混合物有关计算,题目难度中等,试题综合考查学生的得失电子守恒、质量守恒等综合运用和解决复杂问题的能力,是一道考查能力的好题,注意掌握守恒思想在化学计算中的应用.


科目:高中化学 来源: 题型:选择题
| A. | 葡萄糖能水解成乙醇和二氧化碳 | |
| B. | 氨基乙酸、甲醛、乙二醇均可自身或与其他物质发生聚合反应 | |
| C. | 苯酚能跟碳酸钠溶液反应,则苯酚的酸性比碳酸强 | |
| D. | 实验室用溴乙烷在浓硫酸存在并加热条件下制备乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴乙烷与氢氧化钠溶液共煮后,加入硝酸银检验Br- | |
| B. | 用CuSO4溶液除去由电石和饱和食盐水反应生成的乙炔气体中的杂质 | |
| C. | 用苯、2mol/L的硝酸和3mol/L的硫酸制硝基苯 | |
| D. | 将溴乙烷与氢氧化钠的醇溶液共热后产生的气体通入酸性高锰酸钾溶液以检验乙烯的生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

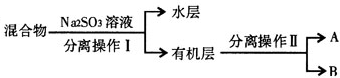
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  验证酸性:H2CO3>H2SiO3 | B. | 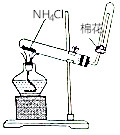 实验室制取氨气 | ||
| C. |  证明石蜡油分解生成的气体是乙烯 | D. | 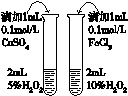 比较不同催化剂对反应速率的影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
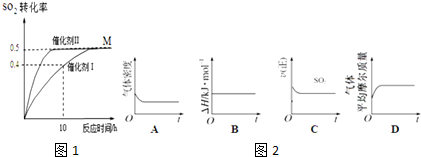
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用酸性高锰酸钾溶液鉴别苯、甲苯和环己烯 | |
| B. | 用燃烧法鉴别乙醇、苯和四氯化碳 | |
| C. | 用水鉴别乙醇、甲苯和溴苯 | |
| D. | 用碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com