
A、碳-12原子
| ||
B、羟基电子式 | ||
C、硫离子结构示意图 | ||
D、CH4S的结构式 |
 ,故B错误;
,故B错误;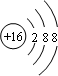 ,故C错误;
,故C错误; ,故D正确;
,故D正确;

科目:高中化学 来源: 题型:
| A、NaNO2溶液的pH大于7 |
| B、向HNO2溶液中加入NaNO2固体,溶液的PH变大 |
| C、常温下0.1mol/LHNO2溶液的pH为2.1 |
| D、用HNO2溶液作导电试验,灯泡很暗 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、纯净的重水(D2O)中,pD=7 |
| B、1 L溶解有0.01 mol DCl的重水溶液,其pD=12.0 |
| C、纯净的重水中,c(D+)=c(OD-) |
| D、1 L溶解有0.01 mol NaOD的重水溶液,其pD=12.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 组别 | 1 | 2 | 3 |
| 盐酸的体积/mL | 50 | 50 | 50 |
| 固体A的质量/g | 3.80 | 6.20 | 7.20 |
| 生成气体体积/mL | 896 | 1344 | 1344 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,22g氧气和26g臭氧混合气体所含氧原子总数为3×6.02×1023 |
| B、1L0.5mol/L的CH3COONa溶液中含有的CH3COO-数为0.5×6.02×1023 |
| C、常温常压下,16g14CH4所含中子数为8×6.02×1023 |
| D、1molCl2发生反应时,转移的电子数一定是2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向NaAlO2溶液中通入足量的CO2气体:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
| B、向FeSO4酸性溶液中加入过氧化氢溶液:2Fe2++H2O2+2H+=2Fe3++2H2O |
| C、向溴水中通入SO2气体:SO2+Br2+2H2O=2H++SO42-+2HBr |
| D、FeS加入稀硫酸中:S2-+2H+=H2S |
查看答案和解析>>
科目:高中化学 来源: 题型:
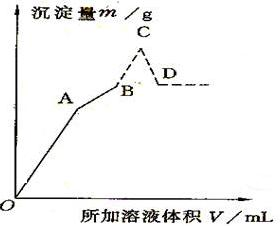
| A | B | C | D | |
| V[Ba(OH)2 (aq)]/ml | ||||
| V[HCl(aq)]/ml | ||||
| M沉淀/g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、已知,现使用1 mol/L KI溶液、0.1 mol/L硫酸和淀粉溶液探究溶液出现蓝色的时间与温度的关系,应先将1 mol/L KI溶液、0.1 mol/L硫酸混合,升温后再加入淀粉溶液 |
| B、将稀氯化铁溶液和稀硫氰化钾溶液混合,溶液呈浅红色,无论向其中加入浓氯化铁溶液还是浓硫氰化钾溶液,红色都会加深 |
| C、向0.1 mol/L的醋酸和饱和硼酸溶液中滴加等浓度的碳酸钠溶液,均有气体生成 |
| D、实验测定酸碱滴定曲线时.要保证整个过程测试和记录pH的间隔相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com