
【题目】配制100mL 0.1mol·L-1的NaOH溶液,下列情况会导致溶液浓度偏高的是
A.用敞口容器称量NaOH且时间过长B.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒
C.定容时仰视观察刻度线D.容量瓶使用前用0.1mol·L-1的NaOH溶液洗涤
科目:高中化学 来源: 题型:
【题目】已知:①Al(OH)3固体的熔点为300℃,电离方程式为H++AlO2-+H2O![]() Al(OH)3
Al(OH)3![]() 3OH-+Al3+;②无水AlCl3晶体易升华,溶于水的电离方程式为AlCl3=Al3++3Cl-;③熔融状态的HgCl2不能导电,稀溶液具有弱的导电能力且可作为手术刀的消毒液,下列关于Al(OH)3、AlCl3和HgCl2的说法正确的是( )
3OH-+Al3+;②无水AlCl3晶体易升华,溶于水的电离方程式为AlCl3=Al3++3Cl-;③熔融状态的HgCl2不能导电,稀溶液具有弱的导电能力且可作为手术刀的消毒液,下列关于Al(OH)3、AlCl3和HgCl2的说法正确的是( )
A.均为强电解质B.均为弱电解质
C.均为离子化合物D.均为共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锑(Sb)在自然界一般以硫化物的形式存在,我国锑的蕴藏量占世界第一。从硫化物中提取单质锑一般是先在高温下将硫化物转化为氧化物,再用碳还原:2Sb2S3+3O2+6Fe=Sb4O6+6FeS①;Sb4O6+6C=4Sb+6CO②。下列说法正确的是( )
A. 反应②说明高温下Sb还原性比C强
B. 反应①中每生成1 mol FeS时,共转移2mol电子
C. 每生成1 mol Sb时,反应①与反应②中还原剂的物质的量之比为4︰3
D. 反应①②中氧化剂分别是Sb2S3、Sb4O6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室通过称量![]() 样品受热脱水前后的质量来测定x值,下列情况会导致测定值偏低的是( )
样品受热脱水前后的质量来测定x值,下列情况会导致测定值偏低的是( )
A. 实验前试样未经干燥B. 试样中含有少量碳酸氢铵
C. 试样中含有少量氯化钠D. 加热过程中有试样迸溅出来
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】探究草酸(H2C2O4)性质,进行如下实验。(已知:室温下,0.1 mol·L1 H2C2O4的pH=1.3)
实验 | 装置 | 试剂a | 现象 |
① |
| Ca(OH)2溶液(含酚酞) | 溶液褪色,产生白色沉淀 |
② | 少量NaHCO3溶液 | 产生气泡 | |
③ | 酸性KMnO4溶液 | 紫色溶液褪色 | |
④ | C2H5OH和浓硫酸 | 加热后产生有香味物质 |
由上述实验所得草酸性质所对应的方程式不正确的是
A. H2C2O4有酸性,Ca(OH)2+ H2C2O4![]() CaC2O4↓+2H2O
CaC2O4↓+2H2O
B. 酸性:H2C2O4> H2CO3,NaHCO3+ H2C2O4![]() NaHC2O4+CO2↑+H2O
NaHC2O4+CO2↑+H2O
C. H2C2O4具有还原性,2![]() +5
+5![]() +16H+
+16H+![]() 2Mn2++10CO2↑+ 8H2O
2Mn2++10CO2↑+ 8H2O
D. H2C2O4可发生酯化反应,HOOCCOOH+2C2H5OH![]() C2H5OOCCOOC2H5+2H2O
C2H5OOCCOOC2H5+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香草醛又名香兰素,是食品和药品的重要原料,其结构简式如图所示。下列有关香草醛的说法中不正确的是( )

A.香草醛可以发生银镜反应
B.在一定条件下1mol香草醛可以与4molH2反应
C.香草醛遇FeCl3溶液可变色
D.香草醛可与NaOH溶液反应,也可与NaHCO3溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)是极易溶于水且不与水发生化学反应的黄绿色气体,沸点为11℃,某小组在实验室中制备ClO2所用装置如图:[已知:SO2+2NaClO3+H2SO4=2ClO2+2NaHSO4]。
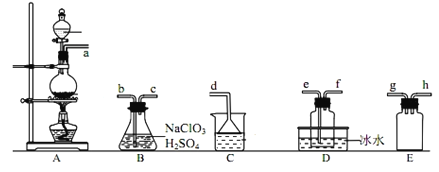
下列说法正确的是( )
A.装置C中装的是饱和食盐水,a流出气体为SO2
B.装置D放冰水的目的是液化二氧化硫防止污染环境
C.连接装置时,导管口a可接h或g,导管口c接e
D.可以选用装置A利用3mo/L盐酸与MnO2反应制备氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(g)+5B(g)![]() 4C(g)+6D(g),在5 L的密闭容器中进行,半分钟后,C的物质的量增加了0.30 mol。下列叙述正确的是( )
4C(g)+6D(g),在5 L的密闭容器中进行,半分钟后,C的物质的量增加了0.30 mol。下列叙述正确的是( )
A. A的平均反应速率是0.010 molL﹣1s﹣1
B. 容器中含D物质的量至少为0.45 mol
C. 容器中A、B、C、D的物质的量的比一定是4∶5∶4∶6
D. 容器中A的物质的量一定增加了0.30 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时在10 mL 0.1mol·L—1Na2CO3溶液中逐滴加入0.1 mol·L—1HCl溶液20 mL,溶液中部分含碳微粒的物质的量随溶液pH的变化如图所示。下列说法不正确的是

A.HCl溶液滴加一半时,溶液pH>7
B.当溶液的pH=8时,溶液中NaHCO3的物质的量浓度为0.1mol·L—1
C.0.1 mol·L—1Na2CO3溶液中c(Na+)+c(H+)=c(OH—)+2c(CO32—)+c(HCO3—)
D.在M点:c(Na+)>c(CO32—)=c(HCO3—)>c(OH—)>c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com