
科目:高中化学 来源: 题型:
25℃ 时,将某一元酸HA和NaOH溶液等体积混合(体积变化忽略不计),测得反应
后溶液的pH如下表:
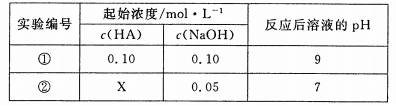
下列判断不正确的是
A、X>0.05
B、将实验①所得溶液加水稀释后,c(OHˉ )/c(A-)变大
C、实验①所得溶液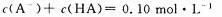
D、实验②所得溶液: 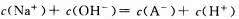
查看答案和解析>>
科目:高中化学 来源: 题型:
钡(Ba)和锶(Sr)及其化合物在工业上有着广泛的应用,它们在地壳中常以硫酸盐的形式存在,BaSO4和SrSO4都是难溶性盐。工业上提取钡和锶时首先将BaSO4和SrSO4转化成难溶弱酸盐。
已知:SrSO4(s) Sr2+(aq)+S(aq) Ksp=2.5×10-7
Sr2+(aq)+S(aq) Ksp=2.5×10-7
SrCO3(s) Sr2+(aq)+C
Sr2+(aq)+C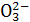 (aq) Ksp=2.5×10-9
(aq) Ksp=2.5×10-9
(1)将SrSO4转化成SrCO3的离子方程式为 ,该反应的平衡常数表达式为 ;该反应能发生的原因是 。
(用沉淀溶解平衡的有关理论解释)
(2)对于上述反应,实验证明增大C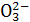 的浓度或降低温度都有利于提高SrSO4的转化率。判断在下列两种情况下,平衡常数K的变化情况(填“增大”“减小”或“不变”):
的浓度或降低温度都有利于提高SrSO4的转化率。判断在下列两种情况下,平衡常数K的变化情况(填“增大”“减小”或“不变”):
①升高温度,平衡常数K将 ;
②增大C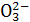 的浓度,平衡常数K将 。
的浓度,平衡常数K将 。
(3)已知,SrSO4和SrCO3在酸中的溶解性与BaSO4和BaCO3类似,设计实验证明上述过程中SrSO4是否完全转化成SrCO3。实验所用的试剂为 ;实验现象及其相应结论为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,用 0.1000 mol·L
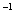 NaOH溶液滴定 20.00mL0.1000 mol·L
NaOH溶液滴定 20.00mL0.1000 mol·L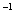
 溶液所得滴定曲线如图。下列说法正确的是
溶液所得滴定曲线如图。下列说法正确的是
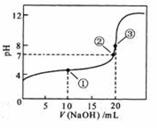
A.点①所示溶液中: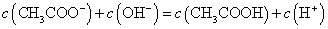
B.点②所示溶液中: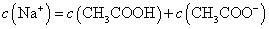
C.点③所示溶液中: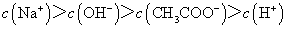
D.滴定过程中可能出现: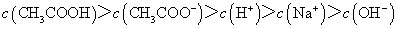
查看答案和解析>>
科目:高中化学 来源: 题型:
氨基甲酸铵(NH2COONH4)是一种白色固体,可用做肥料、灭火剂、洗涤剂等。制备氨基甲酸铵的化学方程式如下:2NH3(g)+CO2(g) NH2COONH4(s) ΔH < 0,已知氨基甲酸铵有以下性质:
NH2COONH4(s) ΔH < 0,已知氨基甲酸铵有以下性质:
a.常温下在干燥的空气中稳定,遇水生成碳酸铵或碳酸氢铵;
b.59℃则可分解成NH3和CO2气体;
用如图I装置制备干燥的氨气,图II装置制备氨基甲酸铵,把制备的干燥的氨气和二氧化碳通入四氯化碳中不断搅拌混合,当生成的氨基甲酸铵晶体悬浮在四氯化碳中较多时停止制备(注:四氯化碳与液体石蜡均为惰性介质)。
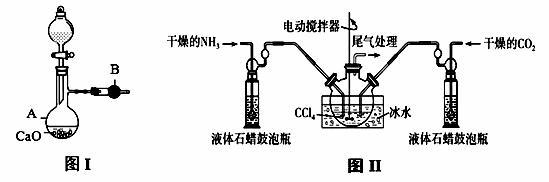
请回答下列问题:
(1)图I中,仪器B的名称 , A中的化学反应方程式是 ;
(2)图II装置中使用冰水的原因是 ;
(3)图II中液体石蜡鼓泡瓶的作用是 ;
(4)从图II反应后的混合物中分离出产品的方法是 ;
A.蒸馏 B.过滤 C.分液 D.结晶
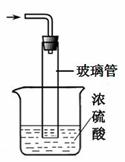
(5)图II装置中,尾气处理装置如图所示,玻璃管的作用 ,浓硫酸的作用是 和防止空气中水蒸气进入反应器使氨基甲酸铵水解;
(6)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品7.82 g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为10.0 g,则样品中氨基甲酸铵的质量分数为 (计算结果精确至0.1%)
查看答案和解析>>
科目:高中化学 来源: 题型:
设计实验方案是科学探究的重要环节。以下化学实验设计中,能达到实验目的的是( )
A.用铜和稀硫酸反应制取硫酸铜溶液
B.用石灰石除去氯化钙溶液中混有的盐酸
C.用氢氧化钠溶液除去二氧化碳中混有的氯化氢气体
D.用酚酞试液检验暴露在空气中的NaOH固体是否变质
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示为实验室中常见的气体制备、净化、收集和性质实验的部分仪器。试根据题目要求,回答下列问题:
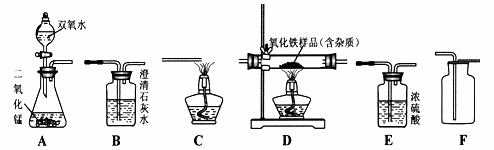
(1)欲在实验室中制备并收集干燥的氧气。
①所选仪器的连接顺序为 (填写仪器序号字母)。
②仪器A中,发生反应的化学方程式为 。
(2)欲用足量纯净的一氧化碳气体测定某不纯氧化铁样品的纯度(杂质不反应),并验证反应中气体生成物的性质。所选仪器的连接顺序为:纯净的一氧化碳气体 →D→B→C。
①仪器C的作用是 。
②仪器D中发生的化学反应方程式为
③反应完全后,计算氧化铁样品的纯度时, 小强同学认为“仪器D中减少的质量等于仪器B中增加的质量”。小丽同学通过称量发现二者质量并不相等。请你分析写出仪器D中减少的是 ________的质量,而仪器B中增加的是 _________的质量。
小强同学认为“仪器D中减少的质量等于仪器B中增加的质量”。小丽同学通过称量发现二者质量并不相等。请你分析写出仪器D中减少的是 ________的质量,而仪器B中增加的是 _________的质量。
查看答案和解析>>
科目:高中化学 来源: 题型:
铀(U)是重要的核工业原料,其中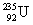 是核反应堆的燃料,下列关于
是核反应堆的燃料,下列关于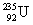 和
和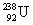 的说法正确的是( )
的说法正确的是( )
A.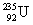 和
和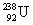 都含有92个中子
都含有92个中子
B.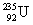 和
和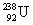 互为同位素
互为同位素
C.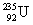 和
和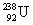 的核外电子数不同
的核外电子数不同
D.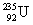 和
和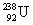 分别含有143和146个质子
分别含有143和146个质子
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.第ⅠA族元素的金属性比第ⅡA族元素的金属性强
B.第ⅥA族元素的氢化物中,稳定性最好的其沸点也最高
C.同周期非金属氧化物对应水化物的酸性从左到右依次增强
D.第2周期元素随族序数的递增其最高化合价也递增
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com