
【题目】探究化合物A(仅含三种短周期元素)的组成和性质,设计并完成如下实验:
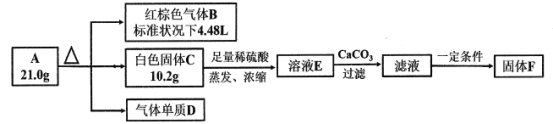
已知:白色固体C既能与强酸反应,也能与强碱反应。
请回答:
(1)写出A受热分解的化学方程式为___________________________________________。
(2)请设计实验方案检验溶液E中所含的阳离子_________________________________。
(3)若固体F中金属元素的百分含量为19.29%,硫为22.86%,氧为57.14%,且300 g/mol<MF<450 g/mol,则F的化学式为____________。
【答案】![]() 取玻璃棒蘸取少量溶液于pH试纸上,成红色,说明有氢离子,另取少量溶液与试管中,加入NaOH溶液,先产生沉淀,后沉淀消失,说明溶液中存在铝离子
取玻璃棒蘸取少量溶液于pH试纸上,成红色,说明有氢离子,另取少量溶液与试管中,加入NaOH溶液,先产生沉淀,后沉淀消失,说明溶液中存在铝离子 ![]()
【解析】
红棕色气体B为二氧化氮,生成的物质的量为0.2mol,白色固体C既能与强酸反应,也能与强碱反应,说明其为氧化铝或氢氧化铝,由于A仅含有三种短周期元素,故C为氧化铝,其物质的量为0.1mol,则气体单质D为氧气,生成的质量为![]() ,则其物质的量为0.05mol,故A的化学式为
,则其物质的量为0.05mol,故A的化学式为![]() 。
。
(1)通过分析可写出A受热分解的化学方程式为![]() ;
;
(2)E中的阳离子为氢离子和铝离子,故可设计两组实验,取玻璃棒蘸取少量溶液于pH试纸上,成红色,说明有氢离子,另取少量溶液与试管中,加入NaOH溶液,先产生沉淀,后沉淀消失,说明溶液中存在铝离子;
(3)根据原子守恒,可知,F中Al元素的质量为![]() ,故F的质量为5.4g÷19.29%=28g,故可算出S的质量为6.40g,O的质量为16.00g,剩余为H的质量,因为300 g/mol<MF<450 g/mol,可得出其化学式为
,故F的质量为5.4g÷19.29%=28g,故可算出S的质量为6.40g,O的质量为16.00g,剩余为H的质量,因为300 g/mol<MF<450 g/mol,可得出其化学式为![]() 。
。


科目:高中化学 来源: 题型:
【题目】对于可逆反应H2(g)+I2(g)![]() 2HI(g),在温度一定下由H2(g)和I2(g)开始反应,下列说法正确的是
2HI(g),在温度一定下由H2(g)和I2(g)开始反应,下列说法正确的是
A.H2(g)的消耗速率与HI(g)的生成速率之比为2:1
B.正、逆反应速率的比值是恒定的
C.达到平衡时,正、逆反应速率相等
D.达到平衡时,H2(g)和I2(g)浓度不在变化且相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案设计及结论均正确的是( )
A.淀粉溶液![]() 水解液
水解液![]() 为蓝。结论:淀粉完全没有水解
为蓝。结论:淀粉完全没有水解
B.淀粉溶液![]() 水解液
水解液![]() 无砖红色沉淀。结论:淀粉完全水解
无砖红色沉淀。结论:淀粉完全水解
C.淀粉溶液![]() 水解液
水解液![]() 中和液
中和液![]() 有砖红色沉淀。结论:淀粉已水解
有砖红色沉淀。结论:淀粉已水解
D.淀粉溶液![]() 水解液
水解液![]() 无现象。结论:淀粉没有水解
无现象。结论:淀粉没有水解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用光伏电池与膜电解法制备Ce(SO4)2溶液的装置如下图所示,下列说法正确的是()
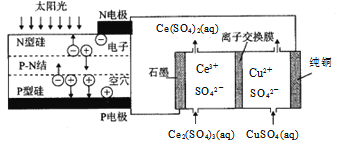
A.该装置工作时的能量形式只有两种
B.石墨电极发生反应:Ce4+ + e- = Ce3+
C.该离子交换膜为阴离子交换膜,SO42-由左池向右池迁移
D.由P电极向N电极转移![]() 电子时,阳极室生成33.2g Ce(SO4)2
电子时,阳极室生成33.2g Ce(SO4)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】材料的发展与应用促进了人类社会的进步
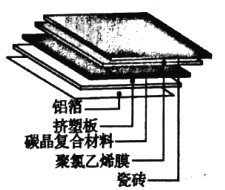
(1)碳晶地暖环保、节能、安全,其构造如图所示。其中属于金属材料的是_____;属于硅酸盐材料的是____;属于高分子材料的是挤塑板和______
(2)吸附材料具有多孔、表面积大的特点,活性炭吸附![]() 的过程中,会伴有C与
的过程中,会伴有C与![]() 的反应,产物为两种常见无毒气体.写出该反应的化学方程式:_____________
的反应,产物为两种常见无毒气体.写出该反应的化学方程式:_____________
(3)![]() 是锂离子电池的一种正极材料,可通过
是锂离子电池的一种正极材料,可通过![]() 与
与![]() 煅烧制备,同时还生成
煅烧制备,同时还生成![]() 和一种单质,写出该反应的化学方程式:________
和一种单质,写出该反应的化学方程式:________
(4)某原电池装置如图所示:
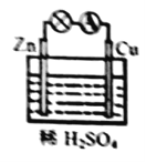
①负极的电极反应式是_______;
②当铜表面析出![]() 氢气(标准状况)时,导线中通过了____
氢气(标准状况)时,导线中通过了____![]() 电子
电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍及其化合物是重要的合金材料和催化剂。请回答下列问题:
(1)基态镍原子的价电子排布式为___________,排布时最高能层的电子所占的原子轨道有__________个伸展方向。
(2)镍能形成多种配合物如正四面体形的Ni(CO)4 和正方形的[Ni(CN)4]2-、正八面体形的[Ni(NH3)6]2+等。下列说法不正确的有_________。
A.CO与CN-互为等电子体,其中CO分子内σ键和π键个数之比为1:2
B.NH3的空间构型为平面三角形
C.Ni2+在形成配合物时,其配位数可能为是4或6
D.Ni(CO)4中,镍元素是sp3杂化
(3)丁二酮肟常用于检验Ni2+:在稀氨水中,丁二酮肟与Ni2+反应生成鲜红色沉淀,其结构如图所示。该结构中,除共价键外还存在配位键和氢键,请在图中用“”表示出氢键。_____
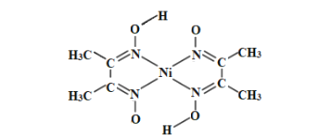
(4)NiO的晶体结构类型与氯化钠的相同,相关离子半径如下表:
![]()
NiO晶胞中Ni2+的配位数为_______,NiO熔点比NaCl高的原因是_______________________。
(5)研究发现镧镍合金LaNix是一种良好的储氢材料。合金LaNix晶体属六方晶系如图a所示,其晶胞如图a中实线所示,如图b所示(其中小圆圈代表La,小黑点代表Ni)。储氢位置有两种,分别是八面体空隙(“![]() ”)和四面体空隙(“
”)和四面体空隙(“![]() ”),见图c、d,这些就是氢原子存储处。
”),见图c、d,这些就是氢原子存储处。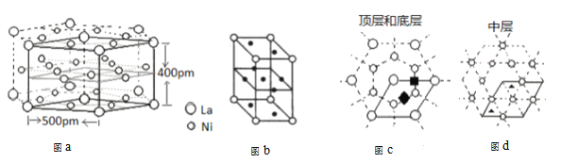
①LaNix合金中x的值为_____;
②LaNix晶胞的密度是________g/cm-3(阿伏伽德罗常数用NA表示,LaNix的摩尔质量用M表示 )
③晶胞中和“![]() ”同类的八面体空隙有______个。
”同类的八面体空隙有______个。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(ClNO)是有机物合成中的重要试剂,其沸点为-5.5℃,易水解。已知:AgNO2微溶于水,能溶于硝酸,AgNO2+HNO3=AgNO3 +HNO2,某学习小组在实验室用Cl2和NO制备ClNO并测定其纯度,相关实验装置如图所示。
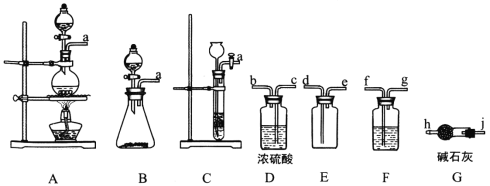
(1)制备Cl2的发生装置可以选用___________(填字母代号)装置,发生反应的化学方程式为_______________________________________________。
(2)欲收集一瓶干燥的氯气,选择合适的装置,其连接顺序为 A→_______→_______→________→_______ (按气流方向,用装置的大写字母表示)。
(3)实验室可用图示装置制备亚硝酰氯:
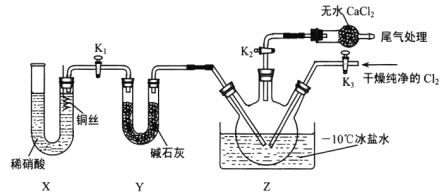
①实验室也可用 B装置制备NO,与B装置相比 X装置的优点为____________。
②检验装置气密性并装入药品,打开K2,然后再打开K3,通入一段时间气体,其目的是______,然后打开K1,当Z中有一定量液体生成时,停止实验。
(4)已知:ClNO 与H2O反应生成HNO2和 HCl。通过以下实验测定ClNO样品的纯度。取Z中所得液体m g 溶于水,配制成250 mL 溶液;取出25.00 mL样品溶于锥形瓶中,以K2CrO4溶液为指示剂,用c molL-1 AgNO3标准溶液滴定至终点,消耗标准溶液的体积为20.00mL。滴定终点的现象是____,亚硝酰氯(ClNO)的质量分数为_____。(已知:Ag2CrO4为砖红色固体; Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=1×10-12)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,一定量混合气体发生反应xA(g)+yB(g)![]() pC(g)+qD(g),平衡时测得B的浓度为1.0 mol·L-1。保持温度不变,将容器的体积压缩到原来的一半,再次达到平衡时,测得B的浓度为1.5 mol·L-1。下列有关判断正确的是
pC(g)+qD(g),平衡时测得B的浓度为1.0 mol·L-1。保持温度不变,将容器的体积压缩到原来的一半,再次达到平衡时,测得B的浓度为1.5 mol·L-1。下列有关判断正确的是
A.x+y<p+qB.气体的平均摩尔质量增大
C.压缩体积时,平衡向逆反应方向移动D.体系中混合气体的平均密度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氮及其化合物的化学用语正确的是
A.氮原子的结构示意图:![]()
B.氨气的电子式:![]()
C.铜与稀硝酸反应的离子方程式:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
D.常温时,氯化铵溶液pH<7的原因:NH4++H2O![]() NH3·H2O+H+
NH3·H2O+H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com