


科目:高中化学 来源: 题型:
| A、SiO2→H2SiO3 |
| B、Fe→FeCl2 |
| C、Cu→CuCl2 |
| D、Fe(OH)2→Fe(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、多数合金的熔点一般比其各成分金属的熔点低 |
| B、多数合金的硬度一般比其各成分金属的硬度小 |
| C、合金的物理性质一般与其各成分金属的物理性质不同 |
| D、合金的化学性质一般与其各成分金属的化学性质不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
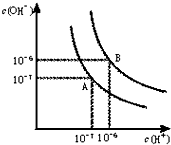 水的电离平衡曲线如图所示.
水的电离平衡曲线如图所示. 查看答案和解析>>
科目:高中化学 来源: 题型:
| A、保持容器体积不变,加入水蒸气 |
| B、将容器的容积缩小一半 |
| C、保持容器容积不变,充入N2使体系压强增大 |
| D、保持压强不变,充入N2使体系容积增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
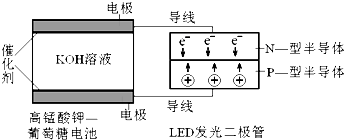
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③④⑥ | B、①②③ |
| C、④⑤⑥ | D、除⑤以外 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com