
�ϳ�����CO��H2����һ����Ҫ�Ļ���ԭ�ϣ��ڻ��������о���ʮ�ֹ㷺����;�����Ʊ������õ�һ�ֹ���������ͼ��ʾ������X��X�����Ҫ�ɷ����ƣ���
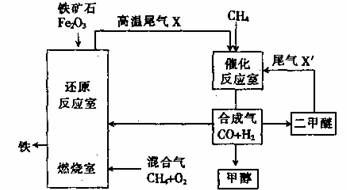
��1���ںϳ���ұ���������������У���ȼ������ͨ�������������Ŀ���� �������������V��CH4����V��O2��Ϊ ��
��2���״��������ѣ�CH3OCH3�������ʱ���Ϊ21���͵�����ȼ�ϣ�������ࡢ��Ч�����������ܡ�
��д���úϳ��������״��Ļ�ѧ����ʽ�� ���ø÷����ϳɼ״�������ŵ��� ��
���úϳ���Ϊԭ�����������ѣ�����ԭ����ȵIJ�ͬ��Ӧ���ﲻ����ͬ����������β����ѭ��ʹ�ã���д����CO��H2Ϊԭ����ȡ�����ѵ����ֲ�ͬ�Ļ�ѧ����ʽ�� ��
��
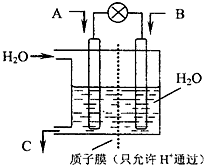
��3��ij��������ͼʹ����ͼ��ʾ�������������״��������ѡ�����������Ϊ�Ƿ���У��������У���˵�����ɣ������У�����������ʲô�ŵ㣿
��
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 ��2010?��������ģ�����ȫ����ڵ������쳣�����������ٴγ�Ϊ���㣮SO2��NOx��CO2�ǶԻ���Ӱ��ϴ�����壬�����ǵĺ������ƺ��������Ż��������滷������Ч;����
��2010?��������ģ�����ȫ����ڵ������쳣�����������ٴγ�Ϊ���㣮SO2��NOx��CO2�ǶԻ���Ӱ��ϴ�����壬�����ǵĺ������ƺ��������Ż��������滷������Ч;����| 3 | 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �ϳ�����CO��H2������Ҫ�Ļ���ԭ�ϣ��ڹ�ҵ���������Ź㷺��Ӧ�ã�
�ϳ�����CO��H2������Ҫ�Ļ���ԭ�ϣ��ڹ�ҵ���������Ź㷺��Ӧ�ã��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��Ӧ���� | ��Ҫ���� | ����1mol�л��� ��H/kJ?mol-1 |
| Cu-ZnO-Cr2O3-MnO��200��400�棬30��40MPa | �״� | -128 |
| Ni��250��500�棬��ѹ | ���飨��ˮ������ | -206.2 |
| FeO-Co-Ni��150��350�棬0.1��3MPa | ����ʯ�� | |
| Ru��150��250�棬10��100MPa | ��̬���� | |
| ThO-ZnO-Al2O3��400��500�棬10��100MPa | �춡�顢������ | |
| Co-Fe��100��200�棬10��20MPa | �����л������� | |
| Rhԭ�Ӵ�������ѹҺ�� | �Ҷ��� ���������ᡢ�Ҵ��� |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢ڢ� | B���ڢۢ� | C���٢ڢܢ� | D���ۢܢ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com