
| A.X、Y一定不是同周期元素 |
| B.X2+的氧化性一定大于Y+ |
| C.由mXa-与nYb+得,m-a=n+b |
| D.若气态氢化物的稳定性HmX大于HnY,则m>n |
科目:高中化学 来源:不详 题型:单选题
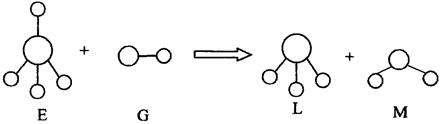
A.E、G、L、M都是10e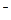 微粒 微粒 | B.L、M都是极性分子 |
| C.L能使紫色石蕊试液变蓝色 | D.E离子中,质子数一定大于中子数 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 元素 | 相关信息 |
| T | T的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子 |
| X | X的原子最外层电子数是其内层电子数的三倍 |
| Y | 在第三周期元素中,Y的简单离子半径最小 |
| Z | T、X、Z组成的36电子的化合物A是家用消毒剂的主要成分 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 元素 | 结构、性质等信息 |
| X | 构成有机物的核心元素,该元素的一种氧化物和气态氢化物都是典型的温室气体 |
| Y | 短周期中(除稀有气体外)原子半径最大的元素,该单质液态时可用作核反应堆的传热介质 |
| Z | 与Y同周期,其最高价氧化物的水化物呈两性 |
| M | 海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
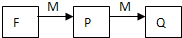
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| A | D | |||
| E | G | M |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.CH4和NH3 | B.H2O和CO2 | C.CO2和HCl | D.H3O+和NH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com