

 .
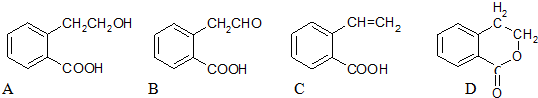
. 分析 A中含有羧基,具有酸性,可发生中和和酯化反应,含有羟基,可发生氧化、消去和取代反应分别生成B、C、D,结合官能团的性质解答该题.
解答 解:(1)由结构简式可知A的分子式为C9H10O3,四种物质均含-COOH,ABCD四种物质中都还有哪些官能团,名称分别是羟基、醛基、碳碳双键、酯基,
故答案为:-COOH;羟基;醛基;碳碳双键;酯基;
(2)A→B为醇的氧化反应,-OH转化为-CHO;A发生消去反应可生成C,C和D分子式相同,但结构不同,为同分异构体关系,
故答案为:氧化反应;消去反应;C和D;
(3)A在催化剂作用下发生氧化反应生成B,反应的方程式为 ,
,
故答案为: ;
;
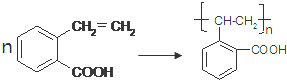
(4)C含有碳碳双键,可发生加聚反应,反应的方程式为 ,
,
故答案为: .
.
点评 本题考查有机物的结构和性质,为高考常见题型,侧重于学生的分析能力的考查,注意把握有机物的官能团的性质,为解答该类题目的关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | N2+3Mg$\frac{\underline{\;点燃\;}}{\;}$Mg3N2 | B. | N2+3H2$?_{催化剂}^{高温、高压}$2NH3 | ||
| C. | 2NO+O2═2NO2 | D. | N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中子数为18的硫离子:${\;}_{16}^{32}$S2- | |
| B. | S2-的结构示意图: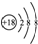 | |
| C. | Na2O2的电子式:Na+[${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$]2-Na+ | |
| D. | 亚硫酸的电离方程式:H2SO3?2H++SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaClO溶液:ClO-+H2O═HClO+OH- | B. | FeCl3溶液:Fe3++3H2O?Fe(OH)3↓+3H+ | ||
| C. | Na2S溶液:S2-+H2O?H2S+2OH- | D. | NH4Cl溶液:NH4++H2O?NH3•H2O+H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
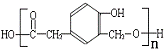 )和某合成鞣剂(
)和某合成鞣剂( 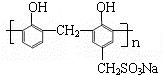 )
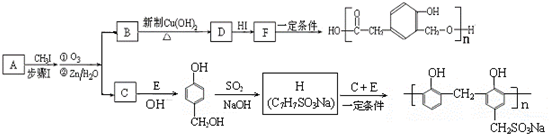
)
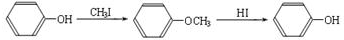
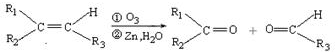 (R1、R2、R3代表烃基)
(R1、R2、R3代表烃基)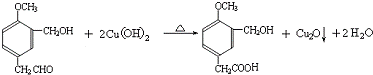 .
. .
.
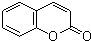 ,写出 X可能的结构简式为
,写出 X可能的结构简式为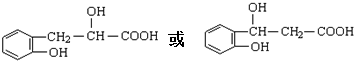 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
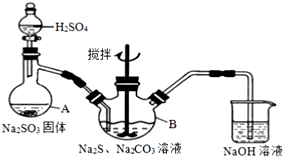 硫代硫酸钠(Na2S2O3)是一种重要的化工产品.某兴趣小组在查阅资料后制备Na2S2O3,结合其性质进行了实验探究.
硫代硫酸钠(Na2S2O3)是一种重要的化工产品.某兴趣小组在查阅资料后制备Na2S2O3,结合其性质进行了实验探究.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 步骤 | 实验操作 | 实验现象及数据 |
| ① | 取wgM粉末溶于过量的盐酸 | 产生气体X在标准状况下的体积为224mL,并得到无色溶液 |
| ② | 向步骤①所得的溶液中滴加氨水,调节pH至6,过滤、洗涤、灼烧、称重 | 固体Y的质量为1.020g |
| ③ | 向步骤②所得的滤液中滴加氢氧化钠溶液,调节pH至12,过滤、洗涤、灼烧、称重 | 固体Z的质量为1.200g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过氧化钠既是氧化剂又是还原剂 | |
| B. | 3摩尔过氧化钠发生反应,有12摩尔电子转移 | |
| C. | 在高铁酸钠中铁为+4价,具有强氧化性,能消毒杀菌 | |
| D. | 高铁酸钠既是氧化产物又是还原产物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com