
【题目】现有①乙酸乙酯和乙酸钠溶液、②溴化钠溶液和溴水的混合液,分离它们的正确方法依次是( )
A. 分液、蒸馏B. 分液、萃取C. 萃取、分液D. 蒸馏、分液
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】由2﹣氯丙烷为主要原料制取1,2﹣丙二醇CH3CH(OH)CH2OH时,经过的反应为( )
A.加成﹣消去﹣取代
B.取代﹣加成﹣消去
C.取代﹣消去﹣加成
D.消去﹣加成﹣取代
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乌洛托品在合成、医药、染料等工业中有广泛用途,其结构式如图所示.将甲醛水溶液与氨水混合蒸发可制得乌洛托品.若原料完全反应生成乌洛托品,则甲醛与氨的物质的量之比为( ) 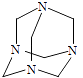
A.1:1
B.2:3
C.3:2
D.2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,下列说法不正确的是 ( )

A. 图Ⅰ表示向AlCl3溶液中滴加氨水至过量
B. 图Ⅱ表示向NaOH溶液中滴加AlCl3溶液至过量且边滴边振荡
C. 图Ⅲ表示向NaAlO2溶液中滴加稀盐酸至过量且边滴边振荡
D. 图Ⅳ表示向NaAlO2溶液中缓慢通入二氧化碳至过量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NO2和N2O4可以相互转化:2NO2(g)N2O4(g)(正反应为放热反应).现将一定量NO2和N2O4的混合气体通入一体积为2L的恒温密闭容器中,反应物物质的量随时间变化关系如图所示,则下列说法错误的是( ) 
A.前10min内用NO2表示的化学反应速率v(NO2)=0.02mol/(Lmin)
B.反应进行至25min时,曲线发生变化的原因可以是向容器中添加NO2(g)
C.若要达到与最后相同的化学平衡状态,在25min时还可以采取的措施是添加N2O4(g)
D.a、b、c、d四个点中,表示化学反应处于平衡状态的点成是b和d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子的检验方法合理的是( )
A. 向某溶液中滴入KSCN溶液呈红色,说明不含Fe2+
B. 向某溶液中通入Cl2,然后再加入KSCN溶液变红色,则原溶液中含有Fe2+
C. 向某溶液中加入NaOH溶液,得到红褐色沉淀,说明溶液中含有Fe3+
D. 向某溶液中加入NaOH溶液得白色沉淀,又观察到颜色逐渐变为红褐色,说明溶液中含有Fe2+,不含有Mg2+
【答案】C
【解析】试题分析:A.KSCN溶液与Fe3+溶液作用的方程式为:Fe3++3SCN-Fe(SCN)3,而Fe2+与KSCN溶液不反应,如果该溶液既含Fe3+,又含Fe2+,滴加KSCN溶液,溶液呈红色,证明存在Fe3+而不能证明没有Fe2+,故A错误;B.若原溶液中含Fe2+,通入Cl2,氯气将Fe2+氧化成Fe3+,滴加KSCN溶液后显红色,若原溶液中不含Fe2+,含有Fe3+,通入Cl2,加入KSCN溶液同样可以变血红色,故B错误;C.加入NaOH溶液,得红褐色沉淀,说明溶液中含有Fe3+,故C正确;D.氢氧化镁为白色沉淀,能被红褐色沉淀掩盖,无法确定,故D错误;故选C。
考点:考查物质的检验及鉴别。
【题型】单选题
【结束】
22
【题目】关于Na2CO3和NaHCO3性质的有关叙述正确的是
A. 在水中的溶解性:Na2CO3<NaHCO3
B. 热稳定性:Na2CO3<NaHCO3
C. 与酸反应的快慢:Na2CO3<NaHCO3
D. Na2CO3不能转化成NaHCO3,而NaHCO3能转化为Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,向100mL含氯化氢14.6g的盐酸溶液里放入5.6g纯铁粉(不考虑反应前后溶液体积的变化),反应开始至2min末收集到氢气1.12L(标况),在此之后,又经过4min铁粉全部溶解.则:
(1)在前2min内用FeCl2表示的平均反应速率是多少?
(2)在后4min内用HCl表示的平均反应速率是多少?
(3)前2min与后4min相比,反应速率哪个较快?为什么?试解释原因.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】密闭容器中进行的可逆反应:aA(g)+bB(g)cC(g)在不同温度(T1和T2)及压强(p1和p2)下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示.下列判断正确的是( ) 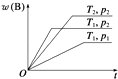
A.T1<T2 , p1<p2 , a+b>c,正反应为吸热反应
B.T1>T2 , p1<p2 , a+b<c,正反应为吸热反应
C.T1<T2 , p1>p2 , a+b<c,正反应为吸热反应
D.T1>T2 , p1>p2 , a+b>c,正反应为放热反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com