
按如图所示装置进行铁和水蒸气反应的实验。
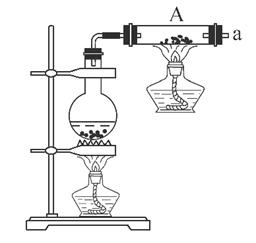
(1)铁粉与水蒸气反应的化学方程式是: ;
(2)为检验生成的气体产物,需从下图选择必要的装置,其正确的连接顺序为(用接口字母表示)a— ,描述能证明气体产物的实验现象_ ;
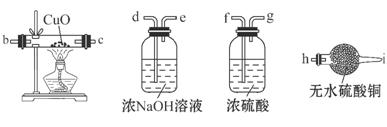
(3)停止反应,待装置冷却后,取出反应过的铁粉混合物,加入过量的稀硫酸充分反应。过滤。简述检验所得滤液中Fe3+的操作方法: ;
(4)经检验上述滤液中不含Fe3+,这不能说明铁粉与水蒸气反应所得产物中不含+3价的铁。原因是(用化学方程式说明): ;
(5)某同学利用上述滤液制取白色的Fe(OH)2沉淀,向滤液中加入NaOH溶液后,观察到生成的白色沉淀迅速变成灰绿色,最后变成红褐色。
①沉淀由白色变为红褐色的化学方程式是: ;
②为了得到白色的Fe(OH)2沉淀,并尽可能使沉淀长时间保持白色,有同学设计如下图所示的装置: 通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法中正确的是________(填序号)。
通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法中正确的是________(填序号)。
A.电源中的a为正极,b为负极 B.可以用NaCl溶液作为电解液
C.A、B两端都必须用铁作电极 D.阴极发生的反应是2H++2e-===H2↑
【知识点】化学实验 J1 J5 C3 F4
【答案解析】(每空2分)(1)Fe+4H2O(g) = Fe3O4+4H2
(2)a—f—g—b—c—h或a—f—g—c—b—h。
黑色的氧化铜变成红色,白色的无水CuSO4变成蓝色
(3)滴加KSCN溶液,溶液变红色
(4)2Fe3++Fe=2Fe2+
(5)①4Fe(OH)2+O2+2H2O═4Fe(OH)3 ②ABD
解析:⑴铁粉与水蒸气反应生成四氧化三铁和氢气
⑵用A盛放铁粉,用B制取水蒸气,铁和水蒸气反应后有部分水蒸气剩余,所以a出来的气体通过浓硫酸进行干燥,洗气瓶中的导气管应该是长进短出,所以a连接f,f连接g,干燥后的氢气进入C装置,可以从b进入,也可以从c进入,所以g可以连接b或c,氧化铜和氢气反应有水蒸气生成,水能使无水硫酸铜变蓝,所以c或b连接h,因此其排序为:afgbch 或afgcbh,当看到无水硫酸铜变蓝,黑色的氧化铜变成红色,则生成的气体是氢气。
⑶Fe3+的检验用KSCN,即滴加KSCN溶液,溶液变红色
⑷固体产物含有四氧化三铁和未反应的铁,四氧化三铁和铁都与盐酸反应生成盐,而且铁与铁离子反应生成Fe2+导致滤液中检验不出Fe3+
⑸①Fe(OH)2被空气中的氧气氧化为氢氧化铁②欲溶液中产生大量的白色沉淀,且较长时间不变色,即利用生成的氢气从上到下排除溶液中的氧气,即B端是阴极,b是负极,阴极材料可以是铁也可以是其它能导电的材料,阴极方程式为:2H++2e-=H2↑,因为氢离子放电破坏水的电离平衡,使氢氧根离子浓度增大,与亚铁离子结合成Fe(OH)2沉淀,金属Fe作阳极,阳极方程式为:Fe-2e-=Fe2+。因此选ABD。
【思路点拨】装置的连接顺序一般是发生装置→除杂→干燥→性质实验→尾气处理。


 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案科目:高中化学 来源: 题型:
下列说法正确的是
A.实验室从海带提取单质碘的方法是:取样→灼烧→溶解→过滤→萃取
B.用乙醇和浓H2SO4制备乙烯时,可用水浴加热控制反应的温度
C.氯离子存在时,铝表面的氧化膜易被破坏,因此含盐腌制品不宜直接放在铝制容器中
D.将(NH4)2SO4、CuSO4溶液分别加入蛋白质溶液,都出现沉淀,表明二者均可使蛋白质变性
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.水的电离过程是吸热过程,升高温度,水的离子积增大、pH减小
B.根据CO2通入漂白粉水溶液中,溶液先变浑浊后澄清,推断SO2通入也有同样现象
C.向1 mL浓度均为0.05 mol·L-1的NaCl、NaI混合溶液中滴加2滴0.01 mol·L-1的
AgNO3溶液,振荡,沉淀呈黄色。结论:Ksp(AgCl)<Ksp(AgI)
D.将Fe(NO3)2晶体溶于稀硫酸,滴加KSCN溶液,通过观察溶液变红确定硝酸亚铁晶体已被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物A~F有如下转化关系:
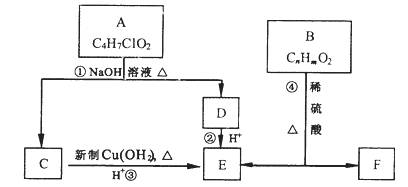
已知一个碳原子上连有两个羟基时不稳定,转化如下:
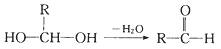
请回答:
(1)A的结构简式为: ;④的反应类型
(2)C与新制Cu(OH)2的化学方程式为
(3)已知B的摩尔质量为162g/mol,完全燃烧的产物中n(CO2):n(H2O)=2:1,B的分子式为 。
(4)F是生产高分子光阻剂的主要原料,特点如下:
①能发生加聚反应 ②含有苯环且苯环上一氯取代物只有两种 ③遇FeCl3显紫色
F与浓溴水反应的化学方程式
B与NaOH反应的化学方程式
(5)F的一种同分异构体G含苯环且能发生银镜反应。写出一种满足条件的G的结构简式
查看答案和解析>>
科目:高中化学 来源: 题型:
正溴丁烷(CH3CH2CH2CH2Br)是一种重要的有机合成工业原料。在实验中可利用下图装置(加热或夹持装置省略)制备正溴丁烷。

制备时的化学反应方程式及有关数据如下:
NaBr+H2SO4=HBr+NaHSO4
C4H9OH+HB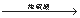 rC4H9Br+H2O
rC4H9Br+H2O
| 物质 | 相对分子质量 | 密度/g·cm-3 | 沸点/℃ | 水中溶解性 |
| 正丁醇 | 74 | 0.80 | 117.3 | 微溶 |
| 正溴丁烷 | 137 | 1.27 | 101.6 | 难溶 |
| 溴化氢 | 81 | --- | --- | 极易溶解 |
实验步骤:在装置A中加入2mL水,并小心加入28mL浓硫酸,混合均匀后冷却至室温。再依次加入18.5mL正丁醇和26g溴化钠,充分摇振后加入沸石,连接气体吸收装置C。将装置A置于石棉网上加热至沸腾,然后调节为小火使反应物保持平稳地回流。一段时间后停止加热,待反应液冷却后,拆去装置B,改为蒸馏装置,蒸出粗正溴丁烷。
请回答下列问题;
(1)仪器A的名称是________,仪器B的作用是________.操作中加入沸石的作用是________.
(2)装置C中盛装的液体是_______________,其作用是____________________.
(3)制备的粗产物正溴丁烷中往往含有水分、正丁醇等杂质,加入干燥剂出去水分后,再由下列操作中的___________制备纯净的正溴丁烷。
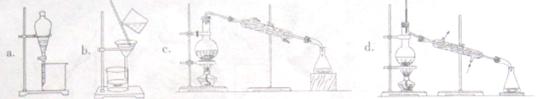
(4)若制备实验的“回流”过程中不采用“调节为小火”,仍采用大火加热回流,则会使产品产率偏_________(填“高”或“低”),试说出其中一种原因:_________________________.
(5)若最终得到13.6g纯净的正溴丁烷,则该实验的产率是_______________(保留三位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
肉桂酸甲酯是常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精。
它的分子式为C10H10O2,且分子中只含有1个苯环,苯环上只有一个取代基。
现测出肉桂酸甲酯的核磁共振氢谱谱图有6个峰,其面积之比为1︰2︰2︰1︰1︰3。利用红外光谱仪可初步检测有机化合物中的某些基团,现测得A分子的红外光谱如下图:
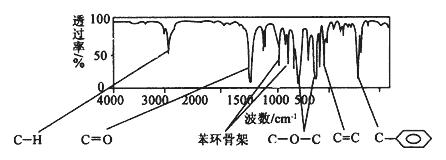
试回答下列问题。
(1)肉桂酸甲酯的结构简式为 。
(2)G为肉桂酸甲酯的一种同分异构体,其分子结构模型如右图所示: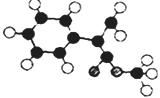
(图中球与球之间连线表示单键或双键)。
用芳香烃A 为原料合成G的路线如下:
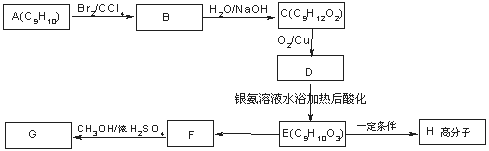
① 化合物E中的官能团有 (填名称)。
② A→B的反应类型是 ,E→F的反应类型是 ,
③ 书写化学方程式
B→C
C→D
E→H
④ 其中E的同分异构体甚多,其中有一类可用通式 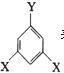 表示
表示
(其中X、Y均不为H),
试写出符合上述通式且能发生银镜反应的四种物质的结构简式:
、
、
查看答案和解析>>
科目:高中化学 来源: 题型:
已知Ba(AlO2)2可溶于水。右图表示的是向A12(SO4) 3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物 质的量y与加人Ba(OH)2的物质的量x的关系。下列有关叙述正确的是
质的量y与加人Ba(OH)2的物质的量x的关系。下列有关叙述正确的是
A.a—b时沉淀的物质的量:A1(OH)3比BaSO4多
B.c—d时溶液中离子的物质的量:AlO2-比Ba2+多
C.a—d时沉淀的物质的量:BaSO4可能小于A1(OH)3
D.d—e时溶液中离子的物质的量:Ba2+不可能等于OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
目前,汽车尾气已成为许多大城市空气的主要污染。汽车尾气中含有CO、NO等多种污染物。
(1)汽车燃料中一般不含氮,尾气中所含的NO产生的原因是 , 化学方程式为 。
(2)治理汽车尾气中NO和CO的一种方法是:在汽车的排气管上装上一个催化转化装置,使NO和CO反应,生成CO2和 N2。反应的化学方程式为 。
(3)下列措施中,能减少或控制汽车尾气污染有效且可行的是 。
① 制定严格的尾气排放标准,并严格执行。 ② 开发清洁能源,如氢能汽车、太阳能汽车等。 ③ 市民出行带防毒面具。 ④ 市民大量移居城市郊区。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com