
| ||
| ||


 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:
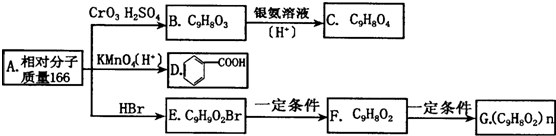
 RCHO
RCHO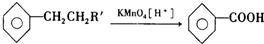
查看答案和解析>>
科目:高中化学 来源: 题型:

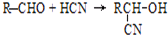


查看答案和解析>>
科目:高中化学 来源: 题型:
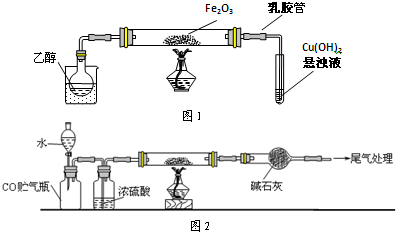
| x |
| y |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、工业可采用火法炼铜:Cu2S+O2═2Cu+SO2 每生成2mol铜,反应共转移6NA个电子 | ||
| B、P4O6的分子结构中只含有单键,且每个原子的最外层都满足8电子结构,则1mol该分子中含有的共价键数目是12NA | ||
| C、一定条件下定容容器中充入3molH2(g)和1mol N2(g)发生反应:3H2(g)+N2(g)?2NH3(g);△H=-QkJ/mol,当该反应放出0.25QkJ的热量时,容器中的氢分子数共有2.25NA | ||
D、标准状况下,定容容器中盛有某气体纯净物,气体密度为ρg?L-1,则该物质相对分子质量为:
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2 4 3 2 2 6 |
| B、0 2 1 0 1 2 |
| C、2 0 1 2 0 2 |
| D、2 2 2 2 1 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 反应时间/min | n(SO2)/mol | n(NO2)/mol |
| 0 | 2.40 | 1.20 |
| 4 | 1.60 | |
| 8 | 0.40 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com