
 盐酸、醋酸和碳酸是化学实验和研究中常用的几种酸.室温下:Ka(CH3COOH)=1.7×10-5 mol/L;H2CO3的电离常数Ka1=4.2×10-7mol•L-1、Ka2=5.6×10-11mol•L-1
盐酸、醋酸和碳酸是化学实验和研究中常用的几种酸.室温下:Ka(CH3COOH)=1.7×10-5 mol/L;H2CO3的电离常数Ka1=4.2×10-7mol•L-1、Ka2=5.6×10-11mol•L-1| 实验编号 | 氢氧化钠溶液的浓度 (mol•L-1) | 滴定完成时,氢氧化钠溶液滴入的体积(mL) | 待测盐酸的体积(mL) |
| 1 | 0.10 | 24.12 | 20.00 |
| 2 | 0.10 | 23.88 | 20.00 |
| 3 | 0.10 | 24.00 | 20.00 |
分析 (1)①NaHCO3是强碱弱酸酸式盐,HCO3-水解程度大于电离程度导致溶液呈碱性;
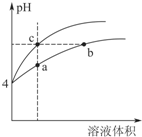
②ab是盐,弱酸根离子水解导致溶液呈碱性;cd是可溶性强碱,溶液中c(OH-)越大,溶液的碱性越强;
(2)醋酸是弱酸,盐酸是强酸,pH相同的醋酸和盐酸,加水稀释过程中醋酸电离出氢离子导致稀释相同倍数时pH醋酸<盐酸,所以pH变化大的是盐酸、变化小的是醋酸,根据图知,上边曲线表示盐酸、下边曲线表示醋酸,
酸抑制水电离,酸中氢离子浓度越大其抑制水电离程度越大;
加水稀释促进醋酸电离,但醋酸电离增大程度小于溶液体积增大程度,所以溶液中c(H+)、c(CH3COOH)、c(CH3COO-)都减小,温度不变,水的离子积常数不变,则溶液中c(OH-)增大;
(3)①如溶液颜色变化且半分钟内不变色,可说明达到滴定终点;
②先判断数据的合理性,求出标准NaOH溶液体积,然后依据c(待测)=$\frac{c(标准).V(标准)}{V(待测)}$求出即可;
(4)①溶液中的离子积Kw=C(H+)×c(OH-)=10-a×10-b=10-(a+b)=10-13;
②根据混合溶液的酸碱性计算氢离子浓度,从而计算溶液的pH.
解答 解:(1)①NaHCO3是强碱弱酸酸式盐,HCO3-水解程度大于电离程度导致溶液呈碱性,水解离子方程式为HCO3-+H2O?H2CO3+OH-,故答案为:HCO3-+H2O?H2CO3+OH-;
②ab是盐,弱酸根离子水解导致溶液呈碱性,碳酸根离子水解程度大于醋酸根离子,所以碱性a>b;cd是可溶性强碱,溶液中c(OH-)越大,溶液的碱性越强,d中氢氧根离子浓度大于c,所以碱性d>c,
碱的碱性大于盐,所以pH大小顺序是d>c>a>b,故答案为:dcab;
(2)醋酸是弱酸,盐酸是强酸,pH相同的醋酸和盐酸,加水稀释过程中醋酸电离出氢离子导致稀释相同倍数时pH醋酸<盐酸,所以pH变化大的是盐酸、变化小的是醋酸,根据图知,上边曲线表示盐酸、下边曲线表示醋酸,
酸抑制水电离,酸中c(H+)越大其抑制水电离程度越大,根据图知,c(H+)a>b=c,所以抑制水电离程度a>b=c,则水的电离程度b=c>a;
加水稀释促进醋酸电离,但醋酸电离增大程度小于溶液体积增大程度,所以溶液中c(H+)、c(CH3COOH)、c(CH3COO-)都减小,温度不变,水的离子积常数不变,则溶液中c(OH-)增大,
a.溶液中c(H+)、c(CH3COOH)、c(CH3COO-)都减小,温度不变,水的离子积常数不变,则溶液中c(OH-)增大,故错误;
b.水稀释促进醋酸电离,但醋酸电离增大程度小于溶液体积增大程度,所以溶液中c(H+) 变小,故正确;c.$\frac{c(C{H}_{3}COOH)c(O{H}^{-})}{c(C{H}_{3}CO{O}^{-})}$=$\frac{c(C{H}_{3}COOH).c({H}^{+}).c(O{H}^{-})}{c(C{H}_{3}CO{O}^{-}).c({H}^{+})}$=$\frac{{K}_{w}}{{K}_{a}}$,温度不变、离子积常数和电离平衡常数不变,所以该比值不变,故错误;
d.加水稀释促进醋酸电离,则醋酸的物质的量减小、氢离子物质的量增大,所以$\frac{c(C{H}_{3}COOH)}{c({H}^{+})}$减小,故正确;
故答案为:b=c>a;bd;
(3)①滴定时,当溶液颜色变化且半分钟内不变色,可说明达到滴定终点,即酚酞在酸中为无色,在碱性溶液中显浅红色,故答案为:最后一滴NaOH溶液加入,溶液由无色恰好变成浅红色且半分钟内不褪色;
②得出V(标准)=$\frac{23.88+24.00+24.12}{3}$=24.00mL,c(待测)=$\frac{0.1mol/L×24.00mL}{20.00mL}$=0.12mol/L,故答案为:0.12mol/L;
c(待测)=$\frac{c(标准).V(标准)}{V(待测)}$求出即可;
(4)①溶液中的离子积Kw=C(H+)×c(OH-)=10-a×10-b=10-(a+b)=10-13,故答案为:10-13;
②混合溶液中c(OH-)=$\frac{(0.4mol/L-0.1mol/L×2)×0.1L}{0.1L×2}$=0.1mol/L,该溶液中c(H+)=$\frac{{K}_{w}}{c(O{H}^{-})}$=$\frac{1{0}^{-13}}{0.1}$mol/L=10-12mol/L,则溶液的pH=-lg10-12=12,
故答案为:12.
点评 本题考查弱电解质的电离、酸碱混合溶液定性判断等知识点,侧重考查计算及分析能力,明确弱电解质电离特点是解本题关键,难点是有关溶液pH的计算,题目难度中等.


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 0.1mol•L-1NaHCO3溶液:H+、Al3+、Cl-、CH3COO- | |
| B. | 0.1mol•L-1CuCl2溶液:K+、NH4+、OH-、S2- | |
| C. | 0.1mol•L-1FeCl2溶液:Na+、NH4+、I-、SO42- | |
| D. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1×1013的溶液:Fe3+、Na+、SO32ˉ、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
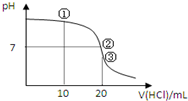 常温下,用0.1000mol/L HCl溶液滴定20.00mL 0.1000mol/L NH3•H2O溶液,滴定曲线如图.下列说法正确的是( )
常温下,用0.1000mol/L HCl溶液滴定20.00mL 0.1000mol/L NH3•H2O溶液,滴定曲线如图.下列说法正确的是( )| A. | ①溶液:c(C1-)>c(NH4+)>c(OH-)>c(H+) | |
| B. | ②溶液:c(NH4+)>c(C1-)>c(OH-)=c(H+) | |
| C. | ③溶液:c(H+)>c(NH3•H2O)+c(OH-) | |
| D. | 滴定过程中可能出现:c(NH3•H2O)>c(NH4+)>c(OH-)>c(Cl-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将SO2通入品红溶液,溶液褪色后加热恢复原色;将SO2通入溴水,溴水褪色后加热也能恢复原色 | |
| B. | 乙酸乙酯的制备实验中,饱和Na2CO3溶液不仅可以降低乙酸乙酯的溶解度,还能吸收挥发出来的乙醇及乙酸 | |
| C. | “中和滴定”实验中,容量瓶和锥形瓶用蒸馏水洗净后即可使用,滴定管和移液管用蒸馏水洗净后,必须干燥或润洗后方可使用 | |
| D. | 除去干燥CO2中混有的少量SO2,可将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
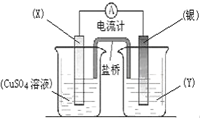 依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
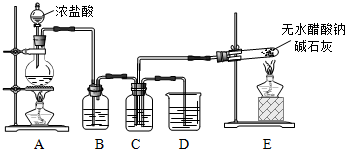
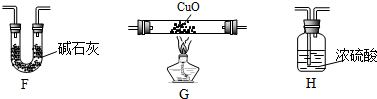
| 装置 | 实验前的质量/g | 实验后的质量/g |
| F | 22.5 | 33.6 |
| H | 42.4 | 51.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 微粒半径:K+>Al3+>S2->Cl- | B. | 离子的还原性:S2->Cl->Br->I- | ||
| C. | 酸性:HClO>H2SO4>H3PO4>H2CO3 | D. | 金属性:K>Ca>Mg>Be |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 呈中性 | B. | 呈碱性 | C. | 呈酸性 | D. | $\frac{c(O{H}^{-})}{c({H}^{+})}$=1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
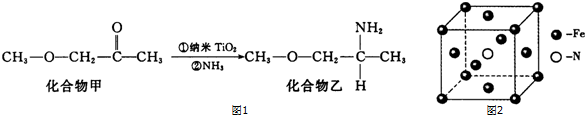
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com