
| A. | 硫原子的原子结构示意图: | |
| B. | 原子核内有10个中子的氧原子:${\;}_{8}^{18}$O | |
| C. | NH4Cl的电子式: | |
| D. | 高氯酸(HClO4)中氯元素的化合价为+5 |
分析 A.硫原子核电荷数、核外电子数都是16,核外电子数不是18;
B.氧元素的质子数为8,中子数为10的氧原子的质量数是18;
C.氯化铵为离子晶体,由氨根离子与氯离子通过离子键结合在一起;
D.高氯酸的Cl处于最高价.
解答 解:A.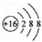 表示的是硫离子,硫原子的核外电子数为16,硫原子结构示意图为:
表示的是硫离子,硫原子的核外电子数为16,硫原子结构示意图为: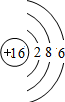 ,故A错误;
,故A错误;
B.含有10个中子的氧原子的质量数为18,该氧原子可以表示为:818O,故B正确;
C.氯化铵是离子化合物,由氨根离子与氯离子构成,电子式为: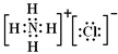 ,故C错误;
,故C错误;
D.高氯酸的Cl处于最高价,为+7价,故D错误,故选B.
点评 本题考查了电子式、原子结构示意图、化学式等表示方法的判断,题目难度中等,注意掌握电子式、原子结构示意图等化学用语的概念及表示方法,明确离子化合物与共价化合物的电子式区别.


科目:高中化学 来源: 题型:解答题

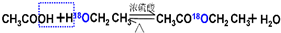 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
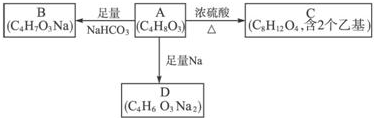
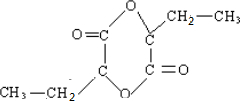 .
.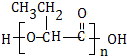 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
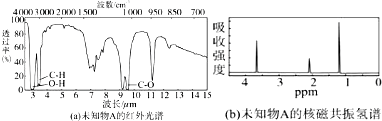
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在元素周期表中,铝的周期数是其主族序数的2倍 | |
| B. | 铝原子的基态电子排布图为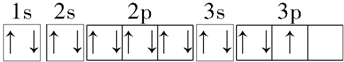 | |
| C. | 同周期,铝、钙所在主族的元素的原子序数之差只为1或11 | |
| D. | 工业上冶炼金属铝的方法是电解熔融的Al2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2Br+NaHS→CH3CH2SH+NaBr | |
| B. | CH3I+CH3ONa→CH3OCH3+NaI | |
| C. | CH3CH2Cl+CH3ONa→CH3CH2ONa+CH3Cl | |
| D. | CH3CH2Cl+CH3CH2ONa→(CH3CH2)2O+NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 滴定次数 | NaOH溶液体积/mL | 滴定消耗滤液体积/mL |
| 1 | 25.00 | 20.02 |
| 2 | 25.00 | 17.10 |
| 3 | 25.00 | 19.98 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com