
在常温、常压下,2体积甲烷和2体积氧气混合,经点燃充分反应后再冷却到原状态,反应前混合气的平均相对分子质量为________,反应后混合气的平均相对分子质量为________.
科目:高中化学 来源: 题型:
| 元素 | 结构或性质信息 |
| T | 原子的L层上s电子数等于p电子数. |
| X | 元素的原子半径是第三周期主族元素中最大的. |
| Y | 空气中含其单质,原子的最外层未成对电子数是该元素所在周期中最多的. |
| Z | 单质常温、常压下是气体.原子的M层上有1个未成对的p电子. |
查看答案和解析>>
科目:高中化学 来源:2010年银川二中高考预测(综合题)化学卷 题型:填空题
A、T、X、Y、z是中学化学常见的四种元素,原子序数依次增大,其结构或性质信息如下表:
| 元素 | 结构或性质信息 |
| T | 基态原子的L层上s电子数等于p电子数 |
| X | 基态原子最外层未成对电子数在该元素所在周期中最多 |
| Y | 基态原子的第一电离能在该元素所在周期中最小 |
| Z | 单质常温、常压下是气体。基态原子的M层上有1个未成对的p电子 |


查看答案和解析>>
科目:高中化学 来源:2015届河南省许昌市五校高二上学期第三次联考化学试卷(解析版) 题型:选择题
下列说法中正确的是( )
A.除去乙烷中混有的乙烯的方法是通氢气在一定条件下反应,使乙烯转化为乙烷
B.苯、溴苯在常温、常压下为无色且密度比水小的液体
C.丙烯与2—丁烯都存在順反异构体
D.苯不能与溴水发生加成反应,也不能被酸性KMnO4溶液氧化
查看答案和解析>>
科目:高中化学 来源:2010-2011学年黑龙江省高三第三次模拟考试(理综)化学部分 题型:填空题
(15分)
M、Q、X、Y、Z是前四周期的5种元素,原子序数依次增大,其结构或性质信息如下表:
|
元素 |
结构或性质信息 |
|
M |
M的一种单质是自然界最硬的物质 |
|
Q |
基态原子最外层未成对电子数在该元素所在周期中最多 |
|
Y |
单质常温、常压下是气体。基态原子的M层上有1个未成对的p电子 |
请回答以下问题:
(1)a.学生甲根据M原子易形成4对共用电子的特点,推出M原子应该具有4个未成对电子。画出基态M原子的价层电子排布图为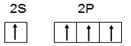 ,请判断对错,并加以解释
,请判断对错,并加以解释
b.M的另一种单质被称为混合型晶体,具有平面层状结构。M原子的杂化方式为________,其晶体中含有的作用力为________________________________________
(2)写出与Q单质分子互为等电子体的常见微粒的化学式(分子、阴离子各1个) 、 ;并写出该阴离子的电子式___________
(3)a.学生乙通过查表,确定Q与Y的电负性接近。但是Q的氢化物分子间能形成氢键,X的氢化物分子间却不易形成氢键,试从结构的角度加以解释:
b.氢键的形成,对分子的沸点影响较大,请判断以下两种互为同分异构体的分子沸点高低:
邻羟基苯甲酸 ______ 对羟基苯甲酸,原因是_________________________________
c.含氧酸的酸性与非羟基氧的个数有关,则Y的四种常见的不同价态含氧酸的酸性由强到弱排序为:
查看答案和解析>>
科目:高中化学 来源:2012届福建省高二下学期期中考试化学试卷 题型:填空题
(16分) 已知 X、Y、Z、Q、R、E六种元素中,原子序数X<Y<Z<Q<R<E,其结构或性质信息如下表。
|
元素 |
结构或性质信息 |
|
X |
原子的L层上s电子数等于p电子数。 |
|
Y |
原子核外的L层有3个未成对电子。 |
|
Z |
在元素周期表的各元素中电负性仅小于氟。 |
|
Q |
单质常温、常压下是气体,原子的M层上有1个未成对的p电子。 |
|
R |
核电荷数是Y与Q的核电荷数之和 |
|
E |
原子序数比R大3 |
请根据信息回答有关问题:
(1)元素Y的原子核外共有 种不同运动状态的电子,有 种不同能级的电子。
(2) X、Y、Z三种元素的第一电离能由高到低的排列次序依次为(写元素符号) 。
(3)X、Z、Q元素均表现最低化合价时的三种氢化物中,沸点由高到低的排列次序依次为(写化学式) 。
(4)R的核外电子排布式为 。R的一种配合物的化学式为RCl3·6H2O。已知0.01 molRCl3·6H2O在水溶液中用过量硝酸银溶液处理,产生0.02 mol AgCl沉淀。此配合物最可能是 。
A.[R(H2O)6]Cl3 B.[R(H2O)5Cl]Cl2·H2O
C.[R(H2O)4Cl2]Cl·2H2O D.[R(H2O)3Cl3]·3H2O
(5)元素E能形成八面体构型的配合物离子[E (YH3) x Q 2]+,则中心原子为(写化学式) ,配位体为(写化学式) ,x 的值为 。
(6) Y的最低价氢化物与Z的一种氢化物反应,生成的两种产物均不污染环境,其反应的化学方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com