
| A. | ①③④② | B. | ①③②④ | C. | ④③②① | D. | ③①④② |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | ①与④ | B. | ②与⑤ | C. | ②与④ | D. | ①、③和④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴加酚酞呈红色的溶液:I-,ClO-,NO3-,Na+ | |
| B. | 含有Fe3+的溶液:K+,Mg2+,SCN-,HSO3- | |
| C. | $\frac{Kw}{c({H}^{+})}$=0.1mol•L-1的溶液:Na+,K+,SiO32-,Br- | |
| D. | 加Al能生成H2的溶液:Na+,K+,CO32-,Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将氯气溶于水,须通入倒置并边缘没入水中的漏斗 | |
| B. | 粉碎结块的硝酸铵,可将药品放入研体中轻轻敲碎 | |
| C. | 洗涤做过银镜反应的试管,先用浓硝酸洗涤,再用自来水冲洗 | |
| D. | 玻璃导管与橡皮导管连接,可使玻璃导管蘸水后边旋转边插入橡皮导管 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaCO3在水中的溶解度很小,其水溶液电阻率很大,所以CaCO3是弱电解质 | |
| B. | CaCO3在水中溶解度很小,但溶于水的CaCO3全部电离,所以CaCO3是强电解质 | |
| C. | 强电解质溶液的导电能力一定强,弱电解质溶液的导电能力一定弱 | |
| D. | 液态SO2不导电,但溶于水后导电,所以SO2是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=1的溶液中:Mg2+,CO${\;}_{3}^{2-}$,SO${\;}_{4}^{2-}$,Na+ | |
| B. | c(Fe3+)=0.1mol•L-1的溶液中:K+,SO${\;}_{4}^{2-}$,OH- | |
| C. | 使石蕊试液变蓝色的溶液中:Mg2+,Cl-,K+ | |
| D. | 使酚酞变红的溶液中:Na+,Cl-,SO${\;}_{4}^{2-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
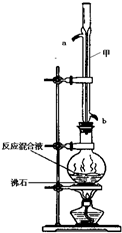 苯甲酸甲酯是一种重要的工业原料,某化学小组采用如图装置,以苯甲酸、甲醇为原料制取苯甲酸甲酯.有关物质的物理性质见下表所示:
苯甲酸甲酯是一种重要的工业原料,某化学小组采用如图装置,以苯甲酸、甲醇为原料制取苯甲酸甲酯.有关物质的物理性质见下表所示:| 苯甲酸 | 甲醇 | 苯甲酸甲酯 | |
| 熔点/℃ | 122.4 | -97 | -12.3 |
| 沸点/℃ | 249 | 64.3 | 199.6 |
| 密度/g.cm-3 | 1.2659 | 0.792 | 1.0888 |
| 水溶性 | 微溶 | 互溶 | 不溶 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 弱酸化学式 | H2SO3 | H2CO3 |
| 电离常数(25℃) | Ka1=1.3×10-2 Ka2=6.3×10-8 | Ka1=4.2×10-7 Ka2=5.6×10-11 |
| A. | c(HCO3-)<c(CO32-) | |
| B. | 两溶液都能使酸性高锰酸钾溶液褪色 | |
| C. | c(HCO3-)>c(HSO3-) | |
| D. | c(CO32-)+c(HCO3-)=c(SO32-)+c(HSO3-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com