
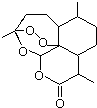
 2015年诺贝尔奖获得者屠呦呦提取的抗疟新药青蒿素的结构简式,用键线式表示如图.
2015年诺贝尔奖获得者屠呦呦提取的抗疟新药青蒿素的结构简式,用键线式表示如图. ,需要在有机合成中引入羟基,引入羟基的反应类型有①②⑤.(选填编号)
,需要在有机合成中引入羟基,引入羟基的反应类型有①②⑤.(选填编号)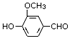 )可用于合成青蒿素,合成天然香草醛的反应如下:
)可用于合成青蒿素,合成天然香草醛的反应如下:
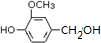 .
. (其中之一).
(其中之一).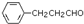 是合成青蒿素的中间原料之一,写出由苯甲醛和氯乙烷为原料,制备苄基乙醛的合成路线流程图(无机试剂任用).已知:羰基α-H可发生反应:
是合成青蒿素的中间原料之一,写出由苯甲醛和氯乙烷为原料,制备苄基乙醛的合成路线流程图(无机试剂任用).已知:羰基α-H可发生反应:
分析 (1)根据青蒿素的结构简式可知其分子式;
(2)在有机合成中引入羟基,可以通过卤代烃的取代、醛与氢气的加成也是还原等方法,不能通过酯化和消去反应得到;
根据C8H10O3的分子式中知,其不饱和度为4,根据 的结构可知C8H10O3中有苯环结构,所以C8H10O3中除了苯环外其它都是单键,所以C8H10O3的结构简式为
的结构可知C8H10O3中有苯环结构,所以C8H10O3中除了苯环外其它都是单键,所以C8H10O3的结构简式为 ,与氢氧化钠反应生成A为
,与氢氧化钠反应生成A为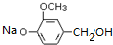 ,A发生催化氧化生成B为
,A发生催化氧化生成B为 ,B再酸化得
,B再酸化得 ,据此回答题 (3)(4)(5);
,据此回答题 (3)(4)(5);
(6)由苯甲醛和氯乙烷为原料,制备苄基乙醛可以用氯乙烷碱性水解得乙醇,再氧化得乙醛,乙醛与苯甲醛在碱性条件下发生信息中的反应得苯丙烯醛,再与氢气催化加成即可得到苄基乙醛.
解答 解:(1)根据青蒿素的结构简式可知其分子式为C15H22O5,
故答案为:C15H22O5;
(2)在有机合成中引入羟基,可以通过卤代烃的取代、醛与氢气的加成也是还原等方法,不能通过酯化和消去反应得到,故选①②⑤;
根据C8H10O3的分子式中知,其不饱和度为4,根据 的结构可知C8H10O3中有苯环结构,所以C8H10O3中除了苯环外其它都是单键,所以C8H10O3的结构简式为
的结构可知C8H10O3中有苯环结构,所以C8H10O3中除了苯环外其它都是单键,所以C8H10O3的结构简式为 ,与氢氧化钠反应生成A为
,与氢氧化钠反应生成A为 ,A发生催化氧化生成B为
,A发生催化氧化生成B为 ,B再酸化得
,B再酸化得 ,
,
(3)根据上面的分析可知,步骤①③的作用是保护酚羟基,避免被氧化,
故答案为:保护酚羟基,避免被氧化;
(4)C8H10O3的结构简式为 ,
,
故答案为: ;
;
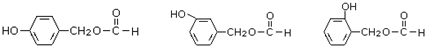
(5)根据条件①有苯环;②能水解;③能发生银镜反应,说明有醛基;④遇FeCl3溶液发生显色反应,说明有酚羟基,则符合条件的天然香草醛的同分异构体的结构简式为 ,
,
故答案为: (其中之一);
(其中之一);
(6)由苯甲醛和氯乙烷为原料,制备苄基乙醛可以用氯乙烷碱性水解得乙醇,再氧化得乙醛,乙醛与苯甲醛在碱性条件下发生信息中的反应得苯丙烯醛,再与氢气催化加成即可得到苄基乙醛,合成路线为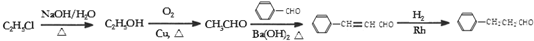 ,
,
故答案为: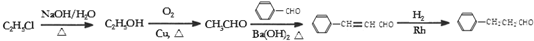 .
.
点评 本题考查了有机物推断与合成,涉及对工艺流程的分析与推断、有机反应类型、官能团、合成工艺流程的设计,难度中等,注意根据转化关系中有机物的结构理解发生的反应.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 在离子化合物中不可能存在非极性共价键 | |
| B. | 由电子定向移动而导电的物质一定是金属晶体 | |
| C. | 有键能很大的共价键存在的物质熔沸点一定很高 | |
| D. | 只含有共价键的物质不一定是共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
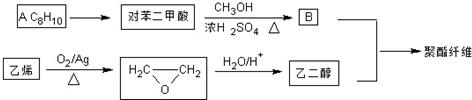
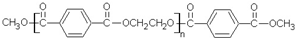 若乙二醇过量,则生成的聚酯纤维可表示为
若乙二醇过量,则生成的聚酯纤维可表示为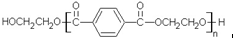 .
.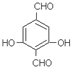 .
. 合成PC的2种单体的中:醇(或酚)的结构简式为
合成PC的2种单体的中:醇(或酚)的结构简式为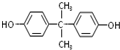 ,酯的名称为碳酸二苯酚酯.
,酯的名称为碳酸二苯酚酯.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 1molN≡N键能与3molH-H键能之和大于6molN-H键能,所以反应为放热 | |
| B. | N2(g)+3H2(g)?2NH3(l)+Q2反应历程的能量变化如曲线Ⅱ,则Q2>Q1 | |
| C. | 选择合适的催化剂,可以降低反应所需温度,Q1值也相应减少 | |
| D. | 2mol氨气的能量高于1mol氮气和3mol氢气的能量之和,所以反应需要高温 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
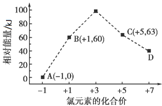 氯的氧化物是氯与氧的二元化合物的总称,也称为氧化氯.目前Cl2O、ClO2、Cl2O7已能制取.有关数据见下表:
氯的氧化物是氯与氧的二元化合物的总称,也称为氧化氯.目前Cl2O、ClO2、Cl2O7已能制取.有关数据见下表:| 化学式 | Cl2O | ClO2 | Cl2O7 |
| 相对分子质量 | 87 | 67.5 | 183 |
| 沸点/℃ | 2 | 9.7 | 81 |
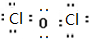 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 都是极性分子 | |
| B. | 都是共价化合物 | |
| C. | 共价分子间的作用力都比化学键弱 | |
| D. | 溶于水的共价分子都能产生自由移动的离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
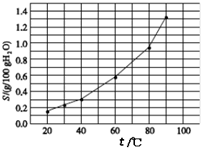
| A. | 温度升高不利于溴酸银的溶解 | |
| B. | 溴酸银的溶解是放热过程 | |
| C. | 若硝酸钾中含有少量溴酸银,可用重结晶方法提纯 | |
| D. | 60℃时,将0.04g溴酸银加入到10g水中,形成的分散系中存在沉淀溶解平衡 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com