
| A. | 将Al2O3固体粉末加到沸水中 | |
| B. | 将CO2气体不断通人到NaAlO2溶液中 | |
| C. | 将过量的金属钠投入到NaAlO2溶液中 | |
| D. | 向340ml 1mol/L NaOH溶液中加入80ml 1mol/L的AlCl3溶液 |
分析 A.Al2O3与水不反应;
B.碳酸酸性比氢氧化铝强,过量CO2通入NaAlO2溶液中生成氢氧化铝白色沉淀;
C.钠和水反应生成氢氧化钠;
D.n(NaOH)=0.34mol,n(AlCl3)=0.08mol,结合反应的离子方程式判断.
解答 解:A.Al2O3不溶于热水中,与水不反应,故A错误;
B.碳酸酸性比氢氧化铝强,过量CO2通入NaAlO2溶液中生成氢氧化铝白色沉淀,故B正确;
C.金属钠投入到NaAlO2,发生的反应为:2Na+2H2O=2NaOH+H2 ↑,没有生成Al(OH)3,故C错误;
D.n(NaOH)=0.34mol,n(AlCl3)=0.08mol,分别发生3OH+Al3+=Al(OH)3↓,AlOH3+OH-=AlO2-+2H2O,所以最终没有沉淀生成,故D错误.
故选B.
点评 本题考查物质之间的化学反应,为高频考点,熟悉复分解反应发生的条件及常见物质的溶解性是解答本题的关键,注意D为易错选项,高频考题,题目难度中等.


 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:选择题
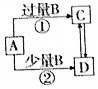
| A. | 若A为AlCl3溶液,B 可能为氨水,反应①的离子方程式为Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | 若A为Fe,B可能为稀HNO3,反应②的离子方程式为3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | |
| C. | 若A为NaOH溶液,B可能为CO2,可用Ca(OH)2溶液鉴定C、D 溶液中的阴离子 | |
| D. | 若A为Cl2,B可能为NH3,实验室可用加热固体C的方法制取NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
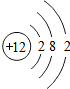 ,其电子所占据的电子层中,能量最高的是M层(填符号).
,其电子所占据的电子层中,能量最高的是M层(填符号).查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑤⑧ | B. | ④⑤⑥ | C. | ①⑤⑦ | D. | ①⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4:3 | B. | 4:5 | C. | 5:4 | D. | 1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6:5 | B. | 3:2 | C. | 15:2 | D. | 3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
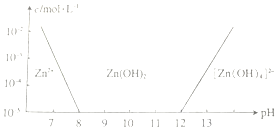 锌及其化合物有着广泛的应用.请回答有关锌及其化合物的有关问题.
锌及其化合物有着广泛的应用.请回答有关锌及其化合物的有关问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com