

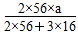 ÷10)g=0.07a g。
÷10)g=0.07a g。

 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.金不溶于任何溶液 |
| B.铜、锌在空气中均能被氧化成对应的氧化物 |
| C.铜锌合金的熔点低于铜或锌的熔点 |
D. 的质子数和中子数之差为34 的质子数和中子数之差为34 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.FeSO4 | B.Fe2(SO4)3 | C.KNO3 | D.HNO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
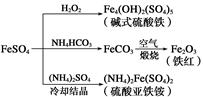
| A.碱式硫酸铁水解能产生Fe(OH)3胶体,可用作净水剂 |
| B.为防止NH4HCO3分解,生产FeCO3需在较低温度下进行 |
| C.可用KSCN溶液检验(NH4)2Fe(SO4)2是否被氧化 |
| D.常温下,(NH4)2Fe(SO4)2在水中的溶解度比FeSO4的大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用FeCl3溶液腐蚀铜制印刷电路板:Fe3++Cu=Fe2++Cu2+ |
| B.NH4HCO3溶液和过量的NaOH溶液相混合:HCO3—+OH-=CO32—+H2O |
| C.向Fe2(SO4)3的酸性溶液中通入足量H2S:Fe3++H2S=FeS↓+2H+ |
| D.FeI2溶液中通入Cl2至I-恰好完全被氧化:2I-+Cl2=I2+2Cl- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
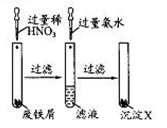
| A.滤液的溶质是Fe(NO3)2 |
| B.该实验中发生的反应都为氧化还原反应 |
| C.沉淀X为Fe(OH)2 |
| D.沉淀X受热分解得到Fe2O3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.塑料容器 | B.铜制容器 | C.铁制容器 | D.陶器 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 取黑色粉末加入稀盐酸 | 溶解,无气泡 | 溶解,有气泡 |
| 2 | 取步骤1中溶液,滴加K3[Fe(CN)6]溶液 | 蓝色沉淀 | 蓝色沉淀 |
| 3 | 取步骤1中溶液,滴加KSCN溶液 | 变红 | 无现象 |
| 4 | 向步骤3溶液中滴加新制氯水 | 红色褪去 | 先变红,后褪色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com