
完成下列表格。
|
分散系 |
分散质粒子大小 |
主要特征 |
举例 |
|
浊液 |
|||
|
溶液 |
|||
|
胶体 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:

| 序号 | 气体 | 装置连接顺序(填字母) | 制作反应的化学方程式 | ||||||
| (1) | 乙烯 | B→D→E B→D→E |
CH3-CH2-OH
CH3-CH2-OH
| ||||||
| (2) | 乙炔 | A→C→E | CaC2+2H2O→Ca(OH)2+C2H2↑ CaC2+2H2O→Ca(OH)2+C2H2↑ |
| 一定条件 |
| (1) |
| 一定条件 |
| (2) |
| 一定条件 |
| (3) |
| 催化剂 |
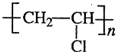
| 催化剂 |
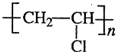
查看答案和解析>>
科目:高中化学 来源: 题型:
| 探究内容 | 实验方案 | 实验现象 | 写出下列离子方程式 |
| 探究Fe2+具有还原性 | 取少量0.1mol?L-1FeCl溶液,加入少量KSCN溶液后,再往溶液中加入少量 新制氯水 新制氯水 |
溶液先不变红,后变为血红色 | ①Fe2+发生的反应: 2Fe2++Cl2=2Fe3++2Cl- 2Fe2++Cl2=2Fe3++2Cl- |
| 探究Fe3+具有氧化性 | 取少量0.1mol?L-1FeCl溶液,加入足量 铁粉 铁粉 后,再往溶液中加入少量KSCN溶液 |
溶液不变为血红色 | Fe3+发生的反应: 2Fe3++Fe=3Fe2+ 2Fe3++Fe=3Fe2+ |
查看答案和解析>>
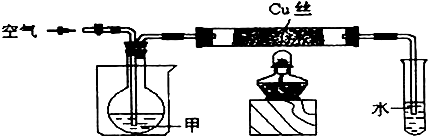
科目:高中化学 来源: 题型:阅读理解
| △ |
| △ |
| 250-350℃ |
| Cu |
| 250-350℃ |
| Cu |
| 操作方法及所用试剂 | 实验现象 |
洗气、水 洗气、水 |
酸性高锰酸钾溶液褪色 酸性高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
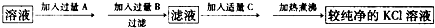
| 目的 | 离子方程式 | |
| 加入过量A | ||
| 加入过量B | ||
| 加热煮沸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 改变条件 | 电离平衡移动方向 | c(H+) | c(CH3COO-) |
| 加水稀释 | |||
| 加少量冰醋酸 | |||
| 加入少量CH3COONa固体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com