
| A.凡是放热反应都是自发的,因为吸热反应都是非自发的 |
| B.自发反应的熵一定增大,非自发反应的熵一定减小 |
C.常温下,反应C(s)+CO2(g)  2CO(g)不能自发进行,则该反应的ΔH>0 2CO(g)不能自发进行,则该反应的ΔH>0 |
| D.反应2Mg(s)+CO2(g)=C(s)+2MgO(s)能自发进行,则该反应的ΔH>0 |
 高效智能课时作业系列答案
高效智能课时作业系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.对于△S>0的反应,若在任何条件下均能自发进行,则该反应△H>0 |
| B.氢氧燃料电池比氢气直接在空气中燃烧能量转换率高 |
| C.合成氨反应N2(g)+3H2(g)?2NH3(g);△H>0,加入催化剂能提高转化率 |
| D.pH=2和pH=4的两种酸混合,其混合后溶液的pH值一定在2~4之间 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.一定温度下,反应MgCl2(l)=Mg(l)+Cl2(g)的ΔH>0 ΔS>0 |
| B.凡是放热反应都是自发的,凡是吸热反应都是非自发的 |
C.常温下,2H2O 2H2↑+O2↑,即常温下水的分解反应是自发反应 2H2↑+O2↑,即常温下水的分解反应是自发反应 |
| D.对于反应H2O2=2H2O+O2↑,加入MnO2或升高温度都能加快O2的生成速率 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.是吸热反应 | B.是放热反应 |
| C.是熵减少的反应 | D.熵增大效应大于能量效应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 CO2(g) ΔH="-393.51" kJ·mol-1
CO2(g) ΔH="-393.51" kJ·mol-1 CO2(g) ΔH="-395.41" kJ·mol-1
CO2(g) ΔH="-395.41" kJ·mol-1| A.石墨转化成金刚石是自发进行的过程 |
| B.金刚石转化成石墨是自发进行的过程 |
| C.金刚石比石墨更稳定 |
| D.金刚石比石墨能量低 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.溶解少量食盐于水中,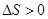 |
B.纯碳和氧气反应生成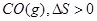 |
C.H2O(g)变成液态水,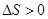 |
D.CaCO3(s)加热分解为CaO和CO2(g),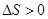 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.是吸热反应 | B.是放热反应 | C.是熵减反应 | D.是熵增效应大于能量效应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2Z(g),减小压强时,下列说法正确的是( )
2Z(g),减小压强时,下列说法正确的是( )| A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动 |
| B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动 |
| C.正、逆反应速率都减小,平衡向逆反应方向移动 |
| D.正、逆反应速率都增大,平衡向正反应方向移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com