
如图是硫酸的试剂标签上的部分内容。某次学生实验需要
0.5 mol·L-1 H2SO4溶液480 mL,若由你来配制所需溶液,请根据
实验室已有的仪器和药品情况回答下列问题:
(1)容量瓶应如何检漏:__________________________________
______________________________________________________。
(2)实验中除量筒、烧杯外还需要的其他仪器:_______________
________________________________________________________________________。
(3)计算所需浓硫酸的体积约为________mL;若将该硫酸与等体积的水混合,所得溶液中溶质的质量分数____49%(填“<”、“=”或“>”)。
(4)配制过程中需先在烧杯中将浓硫酸进行稀释。稀释的操作方法是_______________
________________________________________________________________________。
(5)下列操作会引起所配溶液浓度偏大的是________(填字母)。
A.用量筒量取浓硫酸时,仰视量筒的刻度
B.向容量瓶中转移时,有少量液体溅出
C.定容时仰视刻度线
D.定容后倒置摇匀后再正立时,发现液面低于刻度线
(6)温度计、量筒、滴定管的一部分如图所示,下述读数(虚线所指刻度)及说法正确的是________(填字母)。

A.①是量筒,读数为2.5 mL
B.②是量筒,读数为2.5 mL
C.③是滴定管,读数为2.5 mL
D.①是温度计,读数为2.5 ℃
答案 (1)将瓶塞打开,加入少量水,塞好瓶塞,倒转不漏水,然后正放,把瓶塞旋转180度,再倒转不漏水,则说明该容量瓶不漏水
(2)500 mL容量瓶、玻璃棒、胶头滴管
(3)13.6 >
(4)向烧杯中先加入适量蒸馏水,再将量取的浓硫酸沿烧杯内壁慢慢倒入烧杯中,并用玻璃棒不断搅拌
(5)A (6)BD
解析 (1)容量瓶检漏的方法是加适量水后塞紧瓶塞,倒置不漏水,然后正放,应注意瓶塞要旋转180度,再倒置看是否漏水。(2)由于没有480 mL的容量瓶,故应使用500 mL的容量瓶,另外还需玻璃棒、胶头滴管。(3)由所给浓硫酸标签上的数据易求得该硫酸浓度为18.4 mol·L-1,故配制500 mL 0.5 mol·L-1的稀溶液时约需要13.6 mL浓硫酸。(4)稀释浓硫酸时应将浓硫酸沿器壁慢慢加入到水中,并不断搅拌。(5)仰视量筒时,量筒中实际液面高于看到的液面,导致硫酸取多了,结果偏高;B、C两个选项操作均引起结果偏低。(6)量筒上没有0刻度值,A错;量筒的读数是2.5 mL,B对;滴定管读数时应保留两位小数,C错;只有温度计的0刻度下还有数据,D对。


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源: 题型:
下列各组元素的性质递变情况错误的是( )
A.Li、Be、B原子最外层电子数依次增多
B.P、S、Cl元素最高正价依次升高
C.N、O、F原子半径依次增大
D.Na、K、Rb的金属性依次增强
查看答案和解析>>
科目:高中化学 来源: 题型:
两种硫酸溶液,一种硫酸溶液的物质的量浓度为c1,密度为ρ1;另一种硫酸溶液的物质的量浓度为c2,密度为ρ2,将它们等体积混合后,所得溶液的密度为ρ3,则混合后硫酸的物质的量浓度为 ( )
A. B.
B.
C. D.
D.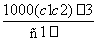
查看答案和解析>>
科目:高中化学 来源: 题型:
配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4的原因是________________;使用的仪器除天平、药匙、玻璃棒、烧杯、量筒外,还需要下图中的________(填字母代号)。

查看答案和解析>>
科目:高中化学 来源: 题型:
若20 g密度为ρ g·cm-3的Ca(NO3)2溶液中含有2 g Ca(NO3)2,则溶液中NO 的物质的量浓度为 ( )
的物质的量浓度为 ( )
A. mol·L-1 B.
mol·L-1 B. mol·L-1
mol·L-1
C.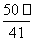 mol·L-1 D.
mol·L-1 D.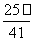 mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与能源、科技、生活、社会密切相关,下列说法不正确的是( )
A.利用太阳能等清洁能源代替化石燃料,有利于节约资源,保护环境
B. 水电站把机械能转化为电能,而核电站把化学能转化为电能
C.化石燃料和植物燃料燃烧时放出的热量均来源于太阳能
D.植物通过光合作用将C02和H20转化为葡萄糖是太阳能转变为化学能的过程
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组性质比较中,正确的是 ( )
①酸性:HClO4>HBrO4>HIO4 ②碱性:Ba(OH)2>Mg(OH)2>Be(OH)2
③氧化性:F>C>O ④还原性:Cl<S<Si
⑤气态氢化物稳定性:HF>HCl>H2S
A、①②③ B、②③④ C、①②④⑤ D、①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
元素X、Y、Z原子序数之和为37,X、Y在同一周期,X+、Z-具有相同的核外电子层结构,下列推测不正确的是( )
A.同族元素中Z的氢化物稳定性最高
B.同周期元素中X的金属性最强
C.原子半径X>Y,离子半径X+>Z-
D.同周期元素中Y的最高价含氧酸的酸性最强
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是周期表中的一部分,根据A-I在周期表中的位置,第(1)~ (4)小题用元素符号或化学式回答,(5)~(8)小题按题目要求回答。
| 族 周期 | I A | Ⅱ A | Ⅲ A | Ⅳ A | Ⅴ A | Ⅵ A | Ⅶ A | O |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
(1)表中元素,化学性质最不活泼的是 ,只有负价而无正价的是 ,氧化性最强的单质是 ,还原性最强的单质是 .
(2)最高价氧化物的水化物碱性最强的是 ,酸性最强的是 ,呈两性的是 .
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的 ,
(4)在B、C、E、F、G、H中,原子半径最大的是 ,
(5)A和D组成化合物的电子式 ,
(6)A和E组成化合物的化学式 ,
(7)用电子式表示B和H组成化合物的形成过程:
。
(8)B的最高价氧化物的水化物和C的最高价氧化物相互反应的离子方程式:
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com