
【题目】能源是人类共同关注的重要问题。页岩气是从页岩层中开采出来的一种非常重要的天然气资源,页岩气的主要成分是甲烷,是公认的洁净能源。
(1)页岩气不仅能用作燃料,还可用于生产合成气(CO和H2)。CH4与H2O(g)通入聚焦太阳能反应器,发生反应CH4(g)+H2O(g)=CO(g)+3H2(g) △H1
已知:①CH4、H2、CO的燃烧热(△H)分别为-a kJmol-1、-b kJmol-1、-c kJmol-1;
②H2O(l)=H2O(g);△H=+d kJmol-1
则△H1=____(用含字母a、b、c、d的代数式表示)kJmol-1。
(2)用合成气生成甲醇的反应为:CO(g)+2H2(g)![]() CH3OH(g) △H2,在10L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如图所示,200℃时n(H2)随时间的变化如表所示:
CH3OH(g) △H2,在10L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如图所示,200℃时n(H2)随时间的变化如表所示:
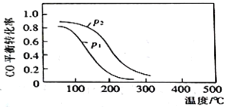
t/min | 0 | 1 | 3 | 5 |
n(H2)/mol | 8.0 | 5.4 | 4.0 | 4.0 |
①△H2____(填“>”“<”或“ = ”)0。
②下列说法正确的是____(填标号)。
a.温度越高,该反应的平衡常数越大
b.达平衡后再充入稀有气体,CO的转化率提高
c.容器内气体压强不再变化时,反应达到最大限度
d.图中压强p1<p2
③03min内用CH3OH表示的反应速率v(CH3OH)=____mol L-1·min-1。
④200℃时,该反应的平衡常数K=__。向上述200℃达到平衡的恒容密闭容器中再加入2mol CO、2mol H2、2mol CH3OH,保持温度不变,则化学平衡___(填“正向”、“逆向”或“不”)移动。
【答案】-a+3b+c–d < cd ![]() (或0.067) 6.25 正向
(或0.067) 6.25 正向
【解析】
(1)根据盖斯定律作答。
(2)①温度对平衡的影响因素为温度升高,化学平衡向吸热方向移动,如果正向移动,反应物的转化率会升高;
②a.平衡常数表示反应进行的程度,当平衡正向移动时平衡常数增大;
b.达平衡后再充入稀有气体,压强增大,但不影响反应物和生成物的浓度,平衡不移动;
c.反应CO(g)+2H2(g)CH3OH(g)在进行的过程中,达到平衡前气体总物质的量在不断变化;
d.在恒温恒容的条件下,增大压强,平衡向气体总物质的量减小的方向移动;
③先根据图表计算在03min内CH3OH的变化浓度,再利用公式v=![]() 计算03min内v(CH3OH);
计算03min内v(CH3OH);
④结合平衡状态和平衡常数的公式计算,向上述200℃达到平衡的恒容密闭容器中再加入2mol CO、2mol H2、2mol CH3OH,保持温度不变,根据此时浓度计算浓度商Qc,再比较Qc与K的关系判断平衡移动方向。
(1)已知:①CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H= a kJmol1,
②H2(g)+![]() O2(g)=H2O(l) △H= b kJmol1,
O2(g)=H2O(l) △H= b kJmol1,
③CO(g)+![]() O2(g)=CO2(g) △H= c kJmol1,
O2(g)=CO2(g) △H= c kJmol1,
④H2O(l)=H2O(g) △H= +d kJmol1,
根据盖斯定律,②×3+③①④可知:CH4(g)+H2O(g)═CO(g)+3H2(g),则△H1=(a+3b+cd) kJmol1,
(2)①由图示可知在恒压条件下,随着温度的升高CO的转化率降低,说明升高温度平衡逆向移动,即正反应为放热反应,△H2<0;
②a. 反应CO(g)+2H2(g)CH3OH(g)正方向为放热反应,升高温度平衡逆向移动,平衡常数减小,a项错误;
b. 达平衡后再充入稀有气体,压强增大,但平衡不移动,CO的转化率不变,b项错误;
c. 反应CO(g)+2H2(g)CH3OH(g)在进行的过程中,达到平衡前气体总物质的量在不断变化,当容器内气体压强不再变化时,说明混合气体的总物质的量不再改变,反应达到平衡,即反应达到最大限度,c项正确;
d. 由图示可知,在恒温恒容的条件下,增大压强,平衡向正方向移动,CO的转化率增大,即图中压强p1<p2,d项正确;
故答案为:cd;
③由图表可知,3min后反应达到平衡状态
CO(g)+2H2(g)CH3OH(g)
起始浓度(mol/L) 0.4 0.8 0
变化浓度(mol/L) 0.2 0.4 0.2
平衡浓度(mol/L) 0.2 0.4 0.2
03min内用CH3OH表示的反应速率v(CH3OH)=![]() =
=![]() (或0.067) molL1min1,
(或0.067) molL1min1,
④由③计算的平衡状态可知,200℃时平衡常数K=![]() =6.25;向上述200℃达到平衡的恒容密闭容器中再加入2mol CO、2mol H2、2mol CH3OH,此时各物质的浓度为c(CO)=0.4mol/L,c(H2)=0.6mol/L,c(CH3OH)=0.4mol/L,保持温度不变,则化学平衡不变,此时Qc=
=6.25;向上述200℃达到平衡的恒容密闭容器中再加入2mol CO、2mol H2、2mol CH3OH,此时各物质的浓度为c(CO)=0.4mol/L,c(H2)=0.6mol/L,c(CH3OH)=0.4mol/L,保持温度不变,则化学平衡不变,此时Qc=![]() <K,则此时平衡向正向移动。
<K,则此时平衡向正向移动。


科目:高中化学 来源: 题型:
【题目】3.2g CH3OH(l)完全燃烧生成液态水和CO2,放出72.576 kJ的热量。下列热化学方程式正确的是
A.CH3OH(l)+![]() O2(g)===CO2(g)+2H2O(l) ΔH = - 72.576 kJ·mol-1
O2(g)===CO2(g)+2H2O(l) ΔH = - 72.576 kJ·mol-1
B.CH3OH(l)+![]() O2(g)===CO2(g)+2H2O(g) ΔH = - 72.576 kJ·mol-1
O2(g)===CO2(g)+2H2O(g) ΔH = - 72.576 kJ·mol-1
C.2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l) ΔH = - 1451.52 kJ·mol-1
D.CH3OH(l)+![]() O2(g)===CO2(g)+2H2O(l) ΔH = + 725.76 kJ·mol-1
O2(g)===CO2(g)+2H2O(l) ΔH = + 725.76 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有pH=2的醋酸溶液甲和pH=2的盐酸乙,请根据下列操作回答问题:
(1)取10mL的甲溶液,加入等体积的水,醋酸的电离平衡___移动(填“向左”、“向右”或“不”);另取10 mL的甲溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中c(H+)/c(CH3COOH)的比值将___(填“增大”、“减小”或“无法确定”)。
(2)相同条件下,取等体积的甲、乙两溶液,各稀释100倍。稀释后的溶液,其pH大小关系为:pH(甲)___pH(乙)(填“大于”、“小于”或“等于)。
(3)各取25 mL的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和至pH=7,则消耗的NaOH溶液的体积大小关系为:V(甲)___V(乙)(填“大于”、“小于”或“等于”)。
(4)取25mL的甲溶液,加入等体积pH=12的NaOH溶液,反应后溶液中c(Na+)、c(CH3COO-)的大小关系为:c(Na+)____c(CH3COO-)(填“大于”、“小于”或“等于”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A(C3H6)是基本有机化工原料。由A制备聚合物C和![]() 的合成路线(部分反应条件略去)如图所示。
的合成路线(部分反应条件略去)如图所示。
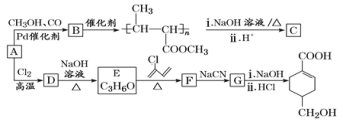
已知:![]() ;R—C
;R—C![]() N
N![]() R—COOH
R—COOH
完成下列填空:
(1)A的名称是__,A一定条件下与水加成,可以得到两种有机物,这两种有机物是__(填“同系物”或“同分异构体”或“同素异形体”)。
(2)C的结构简式为__,D→E的反应类型为__。
(3)E→F的化学方程式为__。
(4)B含有的官能团的名称是__(写名称)。B的同分异构很多,其中相同化学环境的氢原子有三种、比例为6:1:1且能发生银镜反应的是__(写结构简式,任写一种)。
(5)结合题给信息,以乙烯、HBr为起始原料制备丙酸,设计合成路线(其他试剂任选)。__
合成路线流程图示例:CH3CHO![]() CH3COOH
CH3COOH![]() CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种固定烟气中CO2的工艺流程如下:
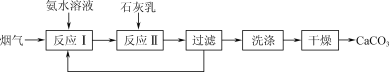
(1) “反应Ⅰ”中,CO2与过量氨水反应的离子方程式为________。
(2) “反应Ⅰ”中,提高烟气中CO2去除率的可行措施有________(填字母)。
a. 采用高温 b. 加快烟气流速 c. 增大氨水浓度
(3) 若测得滤液中c(CO32-)=10-2 mol·L-1,则Ca2+是否沉淀完全?________(填“是”或“否”)。[c(Ca2+)<10-5 mol·L-1时视为沉淀完全;Ksp(CaCO3)=4.96×10-9]
(4) “反应Ⅱ”中,溶液的pH和导电能力变化如图1所示,导电能力初始时快速降低,后来逐渐上升的原因是____________________________________________。
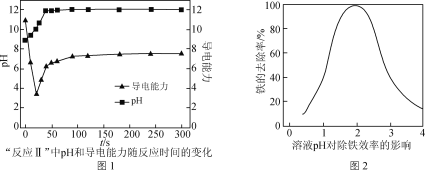
(5) CaCO3可用于调节废水的pH,以除去其中的Fe3+。溶液pH对除铁效率影响如图2所示。
①除铁时应控制溶液的pH为________(填字母)。
a. 0.5~1.5 b. 1.5~2.5 c. 2.5~3.5
② 除铁时pH稍大会生成Fe(OH)3胶体,显著降低除铁效率,其原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以NA代表阿伏加德罗常数,则关于热化学方程式C2H2(g)+ ![]() O2(g) →2CO2(g)+H2O(l) ;ΔH=-1 300 kJ·mol-1的说法中,正确的是( )
O2(g) →2CO2(g)+H2O(l) ;ΔH=-1 300 kJ·mol-1的说法中,正确的是( )
A.当5NA个电子转移时,该反应放出1 300 kJ的能量
B.当1NA个水分子生成且为液体时,吸收1 300 kJ的能量
C.当2NA个碳氧共用电子对生成时,放出1 300 kJ的能量
D.当8NA个碳氧共用电子对生成时,放出1 300 kJ的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X是一种黄酮类化合物的中间体,其结构简式如图所示。下列有关化合物X的说法正确的是( )
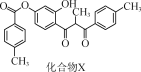
A.分子中所有碳原子共平面
B.分子中存在1个手性碳原子
C.化合物X不能使酸性KMnO4溶液褪色
D.1 mol化合物X最多可与12 mol H2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C、Si、Ge、Sn是同族元素,该族元素单质及其化合物在材料、医药等方面有重要应用。请回答下列问题:
(1)Si的原子核外价电子排布图为___________________________
(2)金刚石的结构是正四面体则其中的碳原子杂化方式是_______________
(3)按要求指出下列氧化物的空间构型、成键方式或性质
①CO2分子的空间构型及碳氧之间的成键方式____________________________;
②CO可以和很多金属形成配合物,如Ni(CO)4,Ni与CO之间的键型为__________;
③乙烯的分子是C2H4,是根据其结构推断是_________分子(填 “极性”或“非极性”)
(4)碳氧键的红外伸缩振动频率与键的强度成正比,已知Ni(CO)4中碳氧键的伸缩振动频率为2060cm-1,CO分子中碳氧键的伸缩振动频率为2143cm-1,则Ni(CO)4中碳氧键的强度比CO分子中碳氧键的强度__________(填字母)
A.强 B.弱 C.相等 D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2C(s)+O2(g)===2CO(g) ΔH=-Q1kJ·mol-1;
C(s)+O2(g)===CO2(g) ΔH=-Q2kJ·mol-1;
S(s)+O2(g)===SO2(g) ΔH=-Q3kJ·mol-1。
CO与镍反应会造成镍催化剂中毒,为防止镍催化剂中毒,工业上常用SO2将CO氧化,二氧化硫转化为单质硫,则该反应的热化学方程式为 ( )
A. SO2(g)+2CO(g)===S(s)+2CO2(g) ΔH=(2Q1-2Q2+Q3) kJ·mol-1
B. S(s)+2CO(g)===SO2(g)+2C(s) ΔH=(Q1-Q3) kJ·mol-1
C. SO2(g)+2CO(g)===S(s)+2CO2(g) ΔH=(Q1-2Q2+Q3) kJ·mol-1
D. SO2(g)+2CO(g)===S(s)+2CO2(g) ΔH=(2Q1-Q2+2Q3) kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com