
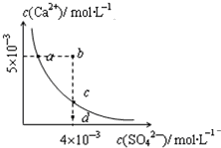
 常温下,Ksp(CaSO4)=9×10-6,常温下CaSO4在水溶液中的沉淀溶解平衡曲线见如图.下列说法不正确的是( )
常温下,Ksp(CaSO4)=9×10-6,常温下CaSO4在水溶液中的沉淀溶解平衡曲线见如图.下列说法不正确的是( )| A. | CaSO4溶解在水中,c(Ca2+)=c(SO42-)=3×10-3mol/L | |
| B. | 在d点溶液中加入一定量的CaCl2可能会有沉淀析出 | |
| C. | a点对应的Ksp等于c点对应的Ksp | |
| D. | b点将有沉淀生成,平衡后溶液中c(SO42-)等于3×10-3mol/L |
分析 A.根据c(Ca2+)=c(SO42-)=$\sqrt{Ksp}$计算;
B.当溶液中Qc=c(Ca2+)×c(SO42-)>Ksp时会析出沉淀;
C.Ksp只与温度有关系;
D.b点Qc>Ksp,会有沉淀生成,结合c(Ca2+)与c(SO42-)的大小关系判断.
解答 解:A.CaSO4溶解在水中,c(Ca2+)=c(SO42-)=$\sqrt{Ksp}$=3×10-3mol/L,故A正确;
B.在d点溶液中加入一定量的CaCl2,当溶液中Qc=c(Ca2+)×c(SO42-)>Ksp时会析出沉淀,所以可能会有沉淀析出,故B正确;
C.Ksp只与温度有关系,a、c两点的温度相同,所以a点对应的Ksp等于c点对应的Ksp,故C正确;
D.根据图示数据,可以看出b点Qc=2×l0-5>Ksp,所以会生成沉淀,平衡向生成沉淀的方向进行,此时溶液中c(SO42-)会小于4×l0-3mol/L,由于c(Ca2+)>c(SO42-),则c(SO42-)小于3×l0-3mol/L,故D错误.
故选D.
点评 本题考查了沉淀溶解平衡的应用、图象分析应用、溶度积计算等,关键是计算混合溶液中钙离子浓度和硫酸根离子浓度,题目难度中等,侧重于考查学生的分析能力和计算能力.


科目:高中化学 来源: 题型:选择题
| A. | 铁丝在纯氧中燃烧 | B. | 红热的铁和水蒸气反应 | ||
| C. | 将Fe2(SO4)3 溶液蒸干后灼烧 | D. | 加热氢氧化铁固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化剂被还原,还原剂被氧化 | |
| B. | 有单质参加或生成的反应一定属于氧化还原反应 | |
| C. | 失电子难的物质,获得电子的能力一定强 | |
| D. | 一种元素被氧化,肯定有另一种元素被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
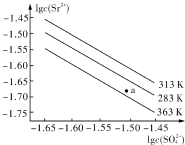
| A. | 温度一定时,KSP(SrSO4)随c(SO42-)的增大而减小 | |
| B. | 三个不同温度中,313K时KSP(SrSO4)最大 | |
| C. | 283K时,图中a点对应的溶液是饱和溶液 | |
| D. | 283K下的SrSO4饱和溶液升温到363K后变为不饱和溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
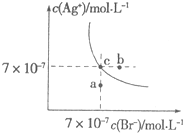 在t℃时,AgBr在水中的沉淀溶解平衡曲线如图所示.又知t℃时AgCl的Ksp=4×10-10,下列说法不正确的是( )
在t℃时,AgBr在水中的沉淀溶解平衡曲线如图所示.又知t℃时AgCl的Ksp=4×10-10,下列说法不正确的是( )| A. | 在t℃时,AgBr的Ksp为4.9×10-13 | |
| B. | 在AgBr饱和溶液中加入NaBr固体,可使溶液由c点到b点 | |
| C. | 图中a点对应的是AgBr的不饱和溶液 | |
| D. | 向组成为c点的溶液中加入等体积的0.1 mol/L的氯化钠溶液,可产生AgCl沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向AgCl沉淀的溶解平衡体系中加入NaCl固体,AgCl的溶解度减小 | |
| B. | 由于Ksp(AgCl)>Ksp(AgI),AgCl 沉淀在一定条件下可转化为AgI沉淀 | |
| C. | 在AgCl沉淀溶解平衡体系中加入蒸馏水,AgCl的Ksp增大 | |
| D. | 向等浓度的NaCl和NaI混合溶液中逐滴加入AgNO3溶液,先出现AgI沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com