
【题目】(1)顺铂(化学名称为顺二氯二氨合铂(II),化学式为PtCl2(NH3)2,相对分子质量为:300)是一种用于治疗癌症的药物,一片顺铂药片所含顺铂的质量为6×10-4g,那么一片顺铂药片中N原子的物质的量___mol;
(2)乙烯气体(C2H4)是石油化工产品之一,也是最重要的有机化工基础原料之一,在标准状况下其密度为___gL-1;
(3)现有一种矿泉水样品,1.0L的该矿泉水含有4.8×10-2gMg2+,则___L矿泉水中含有1mol Mg2+;
(4)某“84消毒液”1000mL,其有效成分为NaClO(式量:74.5),质量分数为14.9%,密度为1.2g/mL,其溶质的物质的量浓度为___molL﹣1;
(5)已知CO和CO2的混合气体7.2g,在标准状况下所占的体积为4.48L。则该混合气体中氧元素的质量为___g;
【答案】4×10-6 1.25 500 2.4 4.8
【解析】
(1)顺铂的摩尔质量=300g/mol,一片顺铂药片中顺铂的物质的量n=![]() =6×10-4g ÷300g/mol=2×10-6mol,一片顺铂药片中顺铂所含氮原子的物质的量=4×10-6mol;
=6×10-4g ÷300g/mol=2×10-6mol,一片顺铂药片中顺铂所含氮原子的物质的量=4×10-6mol;
(2)由M=ρVm可以推出ρ=M÷Vm=28g/mol÷22.4L/mol=1.25 gL-1;
(3)1mol Mg2+的质量是24g, 1.0L的该矿泉水含有4.8×10-2gMg2+,那么24g需要矿泉水的体积是500L;
(4)c=1000ρω÷M=1000×1.2g/mL×14.9%÷74.5g/mol= 2.4 molL﹣1;
(5) 标准状况下,混合气体的物质的量为:4.48L÷22.4L/mol=0.2mol,设CO的物质的量为x,CO2的物质的量为y,则:x28g/mol+y44g/mol=7.2g;x+y=0.2mol,解得:x=0.1mol、y=0.1mol,混合气体中氧元素的质量为m=nM=(0.1mol+0.2mol)×16g/mol=4.8g。


科目:高中化学 来源: 题型:
【题目】巧妙的实验设计有助于更好地解决问题。下列装置不能达到实验目的的是
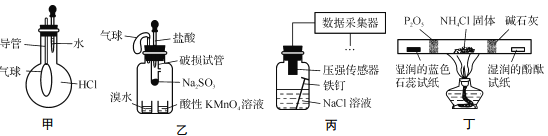
A. 用装置甲验证HCl气体易溶于水
B. 用装置乙验证SO2具有漂白性
C. 用装置丙采集到的压强数据判断铁钉发生析氢腐蚀还是吸氧腐蚀
D. 用装置丁检验NH4Cl分解产生的气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼(N2H4)/空气燃料电池的能量转化率高,装置如图所示。电池放电时,电流由铜极经外电路流向铂极。下列说法错误的是( )

A.在铜极区填充空气
B.放电过程中,OH-向铂极迁移
C.负极反应式为N2H4—4e-=N2+4H+
D.放电过程中,铂极附近溶液pH降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】E是合成某药物的中间体,其一种合成路线如图:

(1)A中含氧官能团的名称是___。
(2)A→B的反应条件和试剂是___。
(3)D→E的反应类型是___。
(4)写出B→C的化学方程式___。
(5)E的分子式为___。
(6)B的环上二溴代物有___种(不考虑立体异构)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢是人们公认的清洁能源,作为低碳和零碳能源正在脱颖而出,氢的获得及以氢为原料的工业生产工艺成为科技工作者研究的重要课题。
(1)工业生产中可利用H2还原CO2制备清洁能源甲醇。
①将一定量的CO2和H2充入到某恒容密闭容器中,测得在不同催化剂作用下,相同时间内CO2的转化率与温度的变化如图所示:
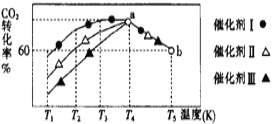
催化效果最好的是催化剂_____________(选填“Ⅰ”“Ⅱ”或“Ⅲ”),该反应在a点达到平衡状态,a点的转化率比b点的高,其原因是______________________________________________________。
②甲醇(CH3OH)燃料电池(NaOH溶液介质)的负极电极反应式 ___________。
(2)利用CO和水蒸气可生产H2,反应的化学方程式:CO(g)+H2O(g)![]() CO2(g)+H2(g)。将不同量的CO(g)和H2O(g)分别通入到体积为2 L的恒容密闭容器中进行如下反应,得到三组数据如下表所示:
CO2(g)+H2(g)。将不同量的CO(g)和H2O(g)分别通入到体积为2 L的恒容密闭容器中进行如下反应,得到三组数据如下表所示:

①该反应的正反应为___________反应(选填“放热”或“吸热” )。
②900℃时,达到平衡时的反应速率v(H2O)=____________,达到平衡时c(H2)=__________(保留2位小数)。
(3)利用废弃的H2S的热分解可生产H2:2H2S(g)![]() 2H2(g)+S2(g)。现将0.20 mol H2S(g)通入到某恒压(压强p=a MPa)密闭容器中,在不同温度下测得H2S的平衡转化率如下图所示:
2H2(g)+S2(g)。现将0.20 mol H2S(g)通入到某恒压(压强p=a MPa)密闭容器中,在不同温度下测得H2S的平衡转化率如下图所示:
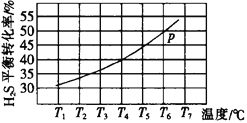
已知:对于气相反应,用某组分(B)的平衡压强(pB)代替物质的量浓度(cB)也可表示平衡常数。 温度为T4℃时,该反应的平衡常数Kp=___________(用a的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化硼(BCl3),主要用作半导体硅的掺杂源或有机合成催化剂,还用于高纯硼或有机硼的制取。某兴趣小组用氯气和硼为原料,采用下列装置(部分装置可重复使用)制备BCl3。

已知:①BCl3的沸点为12.5℃,熔点为-107.3℃;遇水剧烈反应生成硼酸和盐酸;②2B+6HCl ![]() 2BCl3+3H2;③硼与铝的性质相似,也能与氢氧化钠溶液反应。
2BCl3+3H2;③硼与铝的性质相似,也能与氢氧化钠溶液反应。
请回答下列问题:
(1)A装置可用氯酸钾固体与浓盐酸反应制氯气,反应的化学方程式为___________。
(2)装置从左到右的接口连接顺序为a→___________________→j。
(3)装里E中的试剂为___________,如果拆去E装置,可能的后果是____________。
(4)D装置中发生反应前先通入一段时间的氯气,排尽装置中的空气。若缺少此步骤,则造成的结果是_____。
(5)三氯化硼与水能剧烈反应生成硼酸(H3BO3)和白雾,写出该反应的化学方程式________,硼酸也可用电渗析法制备,“四室电渗析法”工作原理如图所示:

则阳极的电极反应式__________________,分析产品室可得到H3BO3的原因________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】理解和应用信息在有机合成中具有重要作用,请依据下列信息回答问题:
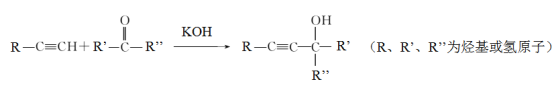
(1)该反应类型为_______________
(2)下列物质能发生上述反应的是______
A.![]() 与
与![]()
B.![]() 与HCHO
与HCHO
C.![]() 与
与![]()
(3)![]() 和
和![]() 在上述条件下能够合成分子式为C8H14O2的物质,该物质的结构简式为________________
在上述条件下能够合成分子式为C8H14O2的物质,该物质的结构简式为________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】迷迭香酸是一种天然抗氧化剂,具有较强的抗氧化活性,能有效降低癌症和动脉硬化的风险。其结构简式为:
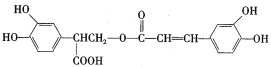
合成路线如下:
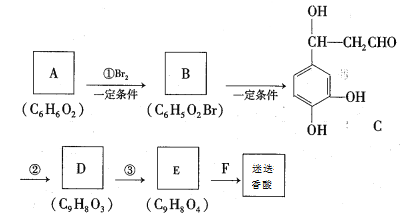
根据题意回答下列问题:
(1)A的结构简式为____________。
(2)①、②的反应类型分别是_____________、_____________。
(3)E的结构简式为__________________
(4)F在一定条件下发生缩聚反应的化学方程式为__________________________________
(5)写出一种与C互为同分异构体,且同时满足下列条件的有机的结构简式________________
①苯环上的一氯代物有2种
②1 mol该有机物能与1 molNaHCO3反应
③能与浓溴水反应,1 mol该有机物消耗3 mol Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,在3支相同体积的试管中分别充有等体积混合的两种气体,它们是①NO和NO2,②NO2和O2,③NO和N2。现将3支试管均倒置于水槽中,充分反应后,试管中剩余气体体积分别为V1、V2、V3,则下列关系正确的是( )
A.V1>V2>V3B.V1>V3>V2
C.V2>V3>V1D.V3>V1>V2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com