
下列关于主族元素电子排布特征的说法正确的是()
A. 主族元素的原子核外电子最后填入的能级是s能级
B. 主族元素的原子核外电子最后填入的能级是s能级或p能级
C. 主族元素的原子核外电子最后填入的能级是d能级或f能级
D. 主族元素的原子核外电子最后填入的能级是s能级或d能级
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
图1为一定量AlCl3溶液中加入NaOH溶液后,产生Al(OH)3白色沉淀的质量与NaOH的物质的量之间的关系曲线.试回答:
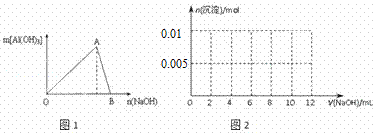
Ⅰ.A点时已参加反应的AlCl3和NaOH的物质的量之比为1比 ;
Ⅱ.B处溶液中存在的浓度最大的离子是 (填离子符号);向B处生成的溶液中通入过量的二氧化碳,可见到的现象是(用离子方程式来表示) ;
Ⅲ.铝铵矾是一种复盐,其主要化学成分为十二水硫酸铝铵NH4Al(SO4)2.12H2O,向该盐的浓溶液中逐滴加入浓NaOH溶液,将发生一系列变化,已知NH4+与AlO2﹣在水溶液中不能大量共存,会发生如下反应:
NH4++AlO2﹣+H2O=Al(OH)3↓+NH3↑.试回答:
(1)写出硫酸铝铵在水溶液中电离的方程式: ;
(2)在逐滴加入NaOH溶液的过程中,产生的现象有:
①溶液中出现白色沉淀;②有刺激性气味的气体放出;③白色沉淀量逐渐增多;④白色沉淀完全消失:⑤白色沉淀逐渐减少.请排出以上各种现象由先到后出现的正确顺序(用序号答) ;
(3)向含有0.1mol NH4Al(SO4)2溶液中逐滴加入5mol•L﹣1NaOH溶液,请在图2中画出生成沉淀的物质的量与加入NaOH溶液体积的关系示意图.
查看答案和解析>>
科目:高中化学 来源: 题型:
已知化合物A(C4Si4H8)与立方烷(C8H8)的分子结构相似,如下图:
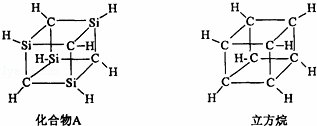
则C4Si4H8的二氯代物的同分异构体数目为( )
|
| A. | 6 | B. | 5 | C. | 4 | D. | 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某元素X的气态氢化物在高温下分解为固态的X单质和H2,分解反应前后气体的质量之比是17:1.下列有关叙述中错误的是()
A. X的阴离子的电子排布式是1s22s22p63s23p6
B. X的最高价氧化物对应的水化物的酸性比砷酸强
C. X的最高价氧化物中,X的质量分数为50%
D. X的气态氢化物的水溶液呈酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D、E 5种元素,它们的核电荷数依次增大,且都小于20.其中只有C、E是金属元素;A和E属同一族,它们原子的最外层电子排布为ns1、B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半.请回答下列问题.
(1)A是 ,B是 ,C是 ,E是 .
(2)B在周期表中位于 区.
(3)写出C元素基态原子核外电子排布式, .
(4)用轨道表示式表示D元素原子的价电子构型 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是()
A. 检验Cl﹣离子的试剂是硝酸银溶液和稀硝酸
B. 检验SO42﹣离子的试剂一般用氯化钡溶液和稀盐酸
C. 检验CO32﹣离子的试剂用盐酸和澄清石灰水
D. 在某溶液中加入BaCl2溶液产生白色沉淀,证明溶液中有SO42﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA表示阿伏加德罗常数,下列叙述中正确的是()
A. 常温常压下,11.2L氧气所含的原子数为NA
B. 在常温常压下,22g二氧化碳中含有的原子数为1.5 NA
C. 在标准状况下,5.6L四氯化碳含有的分子数为0.25NA
D. 在非标准状况下,22.4LO2含有的分子数一定不是NA
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下,下列溶液的离子浓度关系式正确的是()
A. pH=5的H2S溶液中,c(H+)=c(HS﹣)=1×10﹣5 mol•L﹣1
B. pH相同的①CH3COONa、②NaHCO3、③NaClO三种溶液的c(Na+):①>②>③
C. pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
D. pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+c(H+)=c(OH﹣)+c(HC2O4﹣)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com